题目内容
19.元素R的气态氢化物的化学式为HxR,R原子的质子数与中子数相等.在标准状况下,8.5g HxR气体的体积是5.6L.将5.1g HxR气体通入200mL 0.75mol•L-1的CuCl2溶液中恰好完全反应,并生成黑色沉淀.(1)求HxR的相对分子质量.
(2)推断x值,并确定R元素的名称.
分析 (1)根据n=$\frac{V}{{V}_{m}}$计算其物质的量,再根据M=$\frac{m}{n}$计算其摩尔质量,摩尔质量在数值上等于其相对分子质量;
(2)n(HxR)=$\frac{5.1g}{34g/mol}$=0.15mol,而200mL 0.75mol•L-1的CuCl2溶液中氯化铜的物质的量为:0.2L×0.75mol•L-1=0.15mol,二者等物质的量反应,则HxR+CuCl2═CuR↓+2HCl,由氢元素和氯元素质量守恒可知x=2,Ar(R)=32,故R的质量数为32,由此分析解答.
解答 解:(1)标况下,Vm=22.4L/mol,n=$\frac{V}{{V}_{m}}$=$\frac{5.6L}{22.4L/mol}$=0.25mol;M=$\frac{m}{n}$=$\frac{8.5g}{0.25mol}$=34g/mol,摩尔质量在数值上等于其相对分子质量,所以其相对分子质量为34.
答:H2R的相对分子质量为34;
(2)n(HxR)=$\frac{5.1g}{34g/mol}$=0.15mol,而200mL 0.75mol•L-1的CuCl2溶液中氯化铜的物质的量为:0.2L×0.75mol•L-1=0.15mol,二者等物质的量反应,则HxR+CuCl2═CuR↓+2HCl,由氢元素和氯元素质量守恒可知x=2,Ar(R)=32,故R的质量数为32,故R的质量数为32,R的质子数和中子数均为16,R为硫元素,答:x为2,R为硫元素.
点评 本题考查了摩尔质量、质子数与中子数、质量数之间的关系等知识点,难度不大,明确各物理量之间的关系是解答本题的关键.

练习册系列答案
相关题目
9. 已知:①CO(g)+H2O(g)?H2(g)+CO2(g);△H=-41.2kJ/mol
已知:①CO(g)+H2O(g)?H2(g)+CO2(g);△H=-41.2kJ/mol
②CH4(g)+CO2(g)?2CO(g)+2H2(g);△H=+247.3kJ/mol
③CH4(g)+H2O(g)?3H2(g)+CO(g);△H3
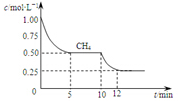
若反应③在1升容器中进行,测得CH4的物质的量浓度随反应时间的变化如图所示.下列有关叙述错误的是( )
 已知:①CO(g)+H2O(g)?H2(g)+CO2(g);△H=-41.2kJ/mol
已知:①CO(g)+H2O(g)?H2(g)+CO2(g);△H=-41.2kJ/mol②CH4(g)+CO2(g)?2CO(g)+2H2(g);△H=+247.3kJ/mol
③CH4(g)+H2O(g)?3H2(g)+CO(g);△H3
若反应③在1升容器中进行,测得CH4的物质的量浓度随反应时间的变化如图所示.下列有关叙述错误的是( )
| A. | △H3=+206kJ/mol | |
| B. | 反应③进行到10min时,改变的外界条件可能是升高温度 | |
| C. | 反应③进行过程中,0~5min这段时间共吸收的热量为103.05kJ | |
| D. | 当反应③平衡后,向容器中通入CH4,平衡向正反应方向移动,CH4的转化率将增大 |
10.下列图示与对应的叙述相符的是( )
| A. | 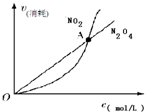 表示在恒容密闭容器中,恒温条件下发生的可逆反应2NO2(g)?N2O4(g),各物质的浓度与其消耗速率之间的关系,其中交点A对应的状态为化学平衡状态 | |
| B. | 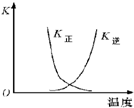 曲线表示反应2A(g)+B(g)?2C(g)△H>0,正、逆反应的平衡常数K随温度的变化 | |
| C. | 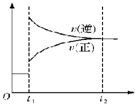 表示对反应2X(g)+Y(g)?Z(s)+3W(g)△H<0 在t1时刻增大压强 | |
| D. | 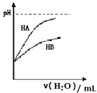 表示常温下,稀释HA、HB两种酸的稀溶液时,溶液pH随加水量的变化,则同浓度的NaA溶液的pH小于NaB溶液pH |
7.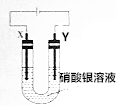 X、Y均为石墨电极,电解硝酸银溶液,实验装置如图所示,电解实验过程中,发现Y极增重的同时,Y极负极产生气泡且气泡由无色变红棕色.已知电流效率等于生成目标产物消耗电子书与电路转移总电子数之比.下列推断正确的是( )
X、Y均为石墨电极,电解硝酸银溶液,实验装置如图所示,电解实验过程中,发现Y极增重的同时,Y极负极产生气泡且气泡由无色变红棕色.已知电流效率等于生成目标产物消耗电子书与电路转移总电子数之比.下列推断正确的是( )
 X、Y均为石墨电极,电解硝酸银溶液,实验装置如图所示,电解实验过程中,发现Y极增重的同时,Y极负极产生气泡且气泡由无色变红棕色.已知电流效率等于生成目标产物消耗电子书与电路转移总电子数之比.下列推断正确的是( )
X、Y均为石墨电极,电解硝酸银溶液,实验装置如图所示,电解实验过程中,发现Y极增重的同时,Y极负极产生气泡且气泡由无色变红棕色.已知电流效率等于生成目标产物消耗电子书与电路转移总电子数之比.下列推断正确的是( )| A. | Y极附近产生的无色气泡是H2 | |
| B. | X极附近电解质溶液中c(H+)会减小 | |
| C. | 若产生2.24L O2(标准状况下)时析出32.4g银,则电流效率为80% | |
| D. | 阴极的副反应为NO3-+3e-+4H+═NO↑+2H2O |
14.在相同条件下能进行如下三个反应:
2A-+B2═2B-+A2
2C-+A2═2A-+C2
2B-+D2═2D-+B2
由此可判断以下分析正确的是( )
2A-+B2═2B-+A2
2C-+A2═2A-+C2
2B-+D2═2D-+B2
由此可判断以下分析正确的是( )
| A. | 氧化性:A2>B2>C2>D2 | B. | 还原性:C->A->B->D- | ||
| C. | 2A-+D2═2D-+A2的反应能进行 | D. | 2C-+B2═2B-+C2的反应不能进行 |
4.符合下列条件的烃的衍生物的结构共有(不考虑立体异构)( )
①分子式符合CxH2x+2Oy
②相对分子质量介于70~100
③氧元素的质量分数为18.18%
④分子中含有2个甲基
⑤能与金属钠反数应放出氢气.
①分子式符合CxH2x+2Oy
②相对分子质量介于70~100
③氧元素的质量分数为18.18%
④分子中含有2个甲基
⑤能与金属钠反数应放出氢气.
| A. | 6种 | B. | 5种 | C. | 4种 | D. | 3种 |
8.下列各组物质与其用途的关系不正确的是( )
| A. | 氢氧化铝:治疗胃酸过多的一种药剂 | |
| B. | 明矾:净水剂 | |
| C. | 烧碱:治疗胃酸过多的一种药剂 | |
| D. | 小苏打:发酵粉主要成分 |
9.研究有机物一般经过以下几个基本步骤:分离、提纯→确定实验式→确定分子式→确定结构式,以下用于研究有机物的方法错误的是( )
| A. | 萃取是常用的有机物提纯方法 | |
| B. | 燃烧法是研究确定有机物成分的有效方法之一 | |
| C. | 对有机物分子红外光谱图的研究有助于确定有机物分子中的官能团 | |
| D. | 核磁共振氢谱通常用于分析有机物的相对分子质量 |