题目内容
18.下列理解不正确的是( )| A. | 化学平衡是一个动态平衡 | |
| B. | 化学平衡研究的对象主要是可逆反应 | |
| C. | 化学反应速率是研究化学反应进行的快慢问题,化学平衡是研究化学反应进行的限度问题 | |
| D. | 化学反应达到平衡时,正反应和逆反应速率相等,是对反应中不同物质而言 |
分析 A.化学平衡是动态平衡,正逆反应速率相等但不等于0;
B.化学平衡研究的对象主要是可逆反应,不适用于不可逆反应;
C.化学反应速率体现化学反应进行的快慢,化学反应的限度体现化学平衡;
D.化学反应达到平衡时,正反应和逆反应速率相等,是对反应中同一物质而言.
解答 解:A.化学平衡是动态平衡,正逆反应速率相等但不等于0,所以处于动态平衡状态,故A正确;
B.化学平衡研究的对象主要是可逆反应,不适用于不可逆反应,可逆反应达到平衡状态时正逆反应速率相等,故B正确;
C.化学反应速率体现化学反应进行的快慢,化学反应限度体现化学平衡,所以化学反应速率是研究化学反应进行的快慢问题,化学平衡是研究化学反应进行的限度问题,故C正确,
D.化学反应达到平衡时,正反应和逆反应速率相等,是对反应中同一物质而言,不同物质之间的正逆反应速率可能相等,故D错误;
故选D.
点评 本题考查化学平衡、化学反应速率等知识点,为高频考点,明确化学平衡研究范围、平衡状态特点等知识点是解本题关键,易错选项是D.

练习册系列答案
相关题目
9.羟基扁桃酸是药物合成的重要中间体,它可由苯酚和乙醛酸反应制得.
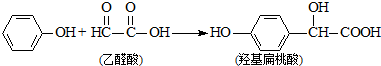
下列有关说法正确的是( )
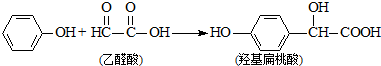
下列有关说法正确的是( )
| A. | 该反应是加成反应 | B. | 苯酚和羟基扁桃酸是同系物 | ||
| C. | 该反应是取代反应 | D. | 乙醛酸不能与 NaOH溶液反应 |
13.用硫酸酸化的CrO3遇酒精后,其颜色会从红色变为蓝绿色,用这个现象可以测得汽车司机是否酒后驾车.反应的方程式为:2CrO3+3CH3CH2OH+3H2SO4═Cr2(SO4)3+3CH3CHO+6H2O,此反应的氧化剂是( )
| A. | H2SO4 | B. | CrO3 | C. | Cr2(SO4)3 | D. | CH3CH2OH |
3.碘及其化合物在合成杀菌剂、药物、化学研究等方面具有广泛用途.
(1)为了探究FeCl3溶液和KI溶液的反应是否存在一定的限度,取5mL 0.5mol•L-1 KI溶液,向其中加入0.1mol•L-1 FeCl3溶液1mL,充分反应.下列实验操作能验证该反应是否存在限度的是D
A.再滴加AgNO3溶液,观察是否有黄色沉淀产生
B.再加入CCl4振荡后,观察下层液体颜色是否变为紫红色
C.再加入CCl4振荡后,取上层清液,滴加AgNO3溶液,观察是否有白色沉淀产生
D.再加入CCl4振荡后,取上层清液,滴加KSCN溶液,观察溶液是否变成血红色
(2)已知1molH2(g)、1molI2(g)、1molHI(g) 分子中化学键断裂时分别需要吸收436kJ、151kJ、300kJ的能量,则氢气和碘蒸气反应生成HI气体的热化学方程式为H2(g)+I2(g)=2HI(g)△H=-13kJ•mol-1
(3)Bodensteins研究了下列反应:2HI(g)?H2(g)+I2(g),在716K,容积固定为2L的密闭容器中,气体混合物中碘化氢的物质的量n(HI)与反应时间t的关系如下表:
0min到20min HI的平均反应速率为0.00225mol•L-1•min-1;
反应到达40min时,剩余HI 的物质的量大于0.82mol(填“>”“<”或“=”).
(1)为了探究FeCl3溶液和KI溶液的反应是否存在一定的限度,取5mL 0.5mol•L-1 KI溶液,向其中加入0.1mol•L-1 FeCl3溶液1mL,充分反应.下列实验操作能验证该反应是否存在限度的是D
A.再滴加AgNO3溶液,观察是否有黄色沉淀产生
B.再加入CCl4振荡后,观察下层液体颜色是否变为紫红色
C.再加入CCl4振荡后,取上层清液,滴加AgNO3溶液,观察是否有白色沉淀产生
D.再加入CCl4振荡后,取上层清液,滴加KSCN溶液,观察溶液是否变成血红色
(2)已知1molH2(g)、1molI2(g)、1molHI(g) 分子中化学键断裂时分别需要吸收436kJ、151kJ、300kJ的能量,则氢气和碘蒸气反应生成HI气体的热化学方程式为H2(g)+I2(g)=2HI(g)△H=-13kJ•mol-1
(3)Bodensteins研究了下列反应:2HI(g)?H2(g)+I2(g),在716K,容积固定为2L的密闭容器中,气体混合物中碘化氢的物质的量n(HI)与反应时间t的关系如下表:
| t/min | 0 | 20 | 40 |
| n(HI) | 1 | 0.91 | n |
反应到达40min时,剩余HI 的物质的量大于0.82mol(填“>”“<”或“=”).
10.可用来鉴别己烯、四氯化碳、甲苯的方法是( )
| A. | 酸性高锰酸钾 | B. | 溴水 | C. | 液溴 | D. | NaOH |
7.有如图所示的装置,当电流表中产生持续电流时,下列说法正确的是( )
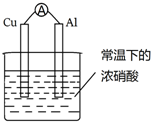

| A. | Cu是原电池的负极 | |
| B. | 电流由Cu电极流出 | |
| C. | 电子由Al沿导线流向Cu | |
| D. | 铝片上的电极反应式为:Al-3e-═Al3+ |
8.某溶液可能含有Cl-、SO42-、CO32-、NH4+、Fe3+、Al3+和K+.取该溶液100mL,加入过量NaOH溶液,加热,得到0.02mol气体,同时产生红褐色沉淀;过滤,洗涤,灼烧,得到1.6g固体;向上述滤液中加足量BaCl2溶液,得到4.66g不溶于盐酸的沉淀.由此可知原溶液中( )
| A. | 至少存在5种离子 | |
| B. | CO32-、Al3+一定不存在,K+可能存在 | |
| C. | SO42-、NH4+一定存在,Cl-可能不存在 | |
| D. | Cl-一定存在 |