题目内容
11.以下判断,结论正确的是( )| 选项 | 项目 | 结论 |
| A | 三种有机化合物:丙烯、氯乙烯、苯 | 分子内所有原子均在同一平面 |
| B | 由溴丙烷水解制丙醇;由丙烯与水反应制丙醇 | 属于同一反应类型 |
| C | 乙烯和苯都能使溴水褪色 | 褪色的原理相同 |
| D | C5H10O2属于羧酸的同分异构体数目 | 共有4种 |
| A. | A | B. | B | C. | C | D. | D |
分析 A、丙烯含有甲基,具有甲烷的四面体结构;
B、由溴丙烷水解制丙醇,属于取代反应;由丙烯与水反应制丙醇,属于加成反应;
C、乙烯与溴水发生加成反应,苯能萃取溴水中的溴;
D、书写丁基-C4H9的同分异构体,-C4H9有几种同分异构体,C5H10O2属于羧酸就有几种同分异构体.
解答 解:A、氯乙烯、苯二者为平面结构,所有原子在同一平面内;丙烯含有甲基,具有甲烷的四面体结构,所有原子不可能在同一平面内,故A错误;
B、由溴丙烷水解制丙醇,属于取代反应,由丙烯与水反应制丙醇,属于加成反应,两者不属于同一反应类型,故B错误;
C、乙烯与溴水发生加成反应,使溴水褪色,苯能萃取溴水中的溴,使溴水褪色,两者的褪色原理不同,故C错误;
D、-C4H9的同分异构体有-CH2CH2CH2CH3、-CH(CH3)CH2CH3、-CH2CH(CH3)2、-C(CH3)3四种,所有C5H10O2属于羧酸有4种同分异构体,故D正确.
故选:D.
点评 本题考查有机物空间结构、同分异构体、有机反应类型、烯烃与苯的性质等,难度中等,注意D选项中同分异构体的书写采取逆向思维书写丁基异构体.

练习册系列答案
相关题目
1.给定条件下,下列选项中所示的物质间转化均能一步实现的是( )
| A. | 粗硅$→_{高温}^{Cl_{2}}$SiCl4 $→_{高温}^{H_{2}}$Si | |
| B. | Mg(OH)2 $\stackrel{盐酸}{→}$NgCl2(ag) $\stackrel{电解}{→}$Mg | |
| C. | Fe2O3 $\stackrel{盐酸}{→}$FeCl3(ag) $\stackrel{蒸发}{→}$无水FeCl3 | |
| D. | Cu $\stackrel{稀硝酸}{→}$NO2 $\stackrel{水}{→}$NO |
2.X、Y、Z、W均是周期表中短周期元素,原子序数逐渐增大,有关信息如下:
(1)甲是X的最高价氧化物,X的最高正价是+4,甲的电子式为 ,X的气态氢化物电子式为
,X的气态氢化物电子式为 .
.
(2)W在元素周期表的位置第三周期第ⅦA族,用电子式表示化合物YW的形成过程
(3)乙是Y的最高价氧化物对应水化物,写出下列反应离子方程式:
①过量的甲通入乙溶液中CO2+OH-=HCO3-
②Z的单质和乙溶液反应2Al+2OH-+2H2O=2AlO2-+3H2↑
③W的单质与乙溶液反应Cl2+2OH-=Cl-+ClO-+H2O.
| 元素 | 相关信息 |
| X | X的原子L层电子数是K层电子数的2倍 |
| Y | Y是短周期元素中原子半径最大的元素(除稀有气体元素外) |
| Z | Z的原子最外层电子数等于电子层数 |
| W | W原子最外层电子数是X、Z原子最外层电子数之和 |
 ,X的气态氢化物电子式为
,X的气态氢化物电子式为 .
.(2)W在元素周期表的位置第三周期第ⅦA族,用电子式表示化合物YW的形成过程

(3)乙是Y的最高价氧化物对应水化物,写出下列反应离子方程式:
①过量的甲通入乙溶液中CO2+OH-=HCO3-
②Z的单质和乙溶液反应2Al+2OH-+2H2O=2AlO2-+3H2↑
③W的单质与乙溶液反应Cl2+2OH-=Cl-+ClO-+H2O.
19.下列离子方程式相对应的化学方程式正确的是( )
| A. | Zn2++2OH-═Zn(OH)2↓;ZnCO3+2NaOH═Zn(OH)3↓+Na2CO3 | |
| B. | Ba2++SO42-═BaSO4↓;Ba(OH)2+H2SO4═BaSO4↓+2H2O | |
| C. | Ag++Cl-═AgCl↓;AgNO3+NaCl═AgCl↓+NaNO3 | |
| D. | Cu+2Ag+═Cu2++2Ag↓;Cu+2AgCl═2Ag+CuCl2 |
3.一种熔融碳酸盐燃料电池原理示意如图.下列有关该电池的说法正确的是( )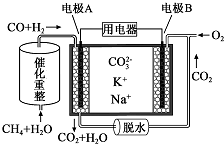

| A. | 反应CH4+H2O$\frac{\underline{催化剂}}{△}$3H2+CO,每消耗1molCH4转移12mol电子 | |
| B. | 电极A上H2参与的电极反应为:H2+2OH--2e-═2H2O | |
| C. | 电池工作时,CO32-向电极B移动 | |
| D. | 电极B上发生的电极反应为:O2+2CO2+4e-═2CO32- |



