题目内容
2.将标准状况下的11.2L甲烷和22.4L氧气混合点燃,恢复到原状况时,气体的体积共11.2 L.分析 根据甲烷燃烧的化学方程式为:CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O可知,11.2L甲烷和22.4L氧气恰好反应,标准状况下水是液态,最后气体为二氧化碳,根据方程式计算二氧化碳体积.
解答 解:甲烷燃烧的化学方程式为CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O,
当温度超过100℃时(即水为气态),反应前后气体的体积不变,
而在标准状况下水是液态,此时根据方程式可知11.2L甲烷与22.4L氧气恰好反应,生成11.2LCO2,最后只剩下CO2,其体积为11.2L,
故答案为:11.2.
点评 本题考查了物质的量的计算、化学方程式的计算,题目难度不大,明确发生反应实质为解答关键,试题培养了学生的分析能力及化学计算能力.

练习册系列答案
相关题目
13.下列说法不正确的是( )
| A. | 向滴有酚酞的水中加入过量Na2O2粉末并振荡,溶液由无色变红又变无色 | |
| B. | 钠的化学性质非常活泼,钠元素只能以化合态存在于自然界 | |
| C. | 将一小粒金属钠投入水和苯的混合体系中,钠在苯与水的界面处反应并可能作上、下跳动 | |
| D. | 某物质灼烧时,焰色反应为黄色,该物质一定只含钠元素 |
10.下列叙述正确的是( )
| A. | 碳族元素都是非金属元素,其非金属性随核电荷数的增加而减弱 | |
| B. | 石英、水晶、硅石的主要成分都是二氧化硅 | |
| C. | 二氧化硅的化学性质活泼,能与任意的酸、碱发生反应 | |
| D. | 碳族元素的单质都有导电性 |
17.两个相同的容器中,一个盛有CO2气体,另一个盛有H2和Cl2的混合气体,同温同压下,两容器内的气体一定具有相同的( )
| A. | 原子数 | B. | 分子数 | C. | 质量 | D. | 密度 |
7.在1gO2和1gO3中( )
| A. | 所含原子数不相同 | B. | 所含分子数相同 | ||
| C. | 物质的量相同 | D. | 所含质子数相同 |
14.肼(N2H4)是一种高能燃料,常温下是液体,燃烧产生巨大能量,可作为航天火箭的推动力.下列叙述中正确的是( )
| A. | N2H4的摩尔质量为32 | |
| B. | 1 molN2H4的质量为32 g•mol-1 | |
| C. | 在标准状况下,1 mol N2H4的体积约为22.4L | |
| D. | 6.02×1023个N2H4分子的质量为32g |
11.燃烧由CH4和C3H8组成的混合气体,生成3.52gCO2和1.98gH2O.此混合气体中CH4与C3H8的体积比为( )
| A. | 1:5 | B. | 1:2 | C. | 3:2 | D. | 2:1 |
12.对于有机物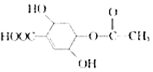 的叙述中不正确的是( )
的叙述中不正确的是( )
 的叙述中不正确的是( )
的叙述中不正确的是( )| A. | 该物质能发生水解反应,1 mol该有机物能与2mo1的NaOH反应 | |
| B. | 该物质可使溴水褪色 | |
| C. | 该物质与Na2CO3溶液反应放出CO2 | |
| D. | 该物质遇FeCl3溶液显色 |