题目内容
在0.5molNa2SO4中含有Na+的数目为6.02×1023个 .(判断对错)
考点:物质的量的相关计算
专题:计算题
分析:根据化学式为Na2SO4,利用硫酸钠的物质的量来确定钠离子的物质的量,再利用N=n×NA来计算钠离子的数目.
解答:
解:0.5molNa2SO4中钠离子的物质的量为0.5mol×2=1mol,
则由N=n×NA可知,则钠离子的个数为1mol×6.02×1023mol-1=6.02×1023,
故答案为:√.
则由N=n×NA可知,则钠离子的个数为1mol×6.02×1023mol-1=6.02×1023,
故答案为:√.
点评:本题考查有关阿伏伽德罗常数的计算,比较基础,关键是确定物质与所含微粒关系,注意对公式的理解与应用.

练习册系列答案
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案
相关题目
常温下,下列各组离子在指定溶液中能大量共存的是( )
| A、pH=1的溶液中:NH4+、Na+、I-、NO3- |
| B、由水电离的c(H+)=1×10-14mol/L的溶液中:Ca2+、K+、Cl-、HCO3- |
| C、c(Fe3+)=0.1mol/L的溶液中:K+、ClO-、SO42-、SCN- |
| D、能使甲基橙变红的溶液中:NH4+、Al3+、NO3-、Cl- |
1g O2和1g O3中( )
| A、所含原子数相同 |
| B、所含分子数相同 |
| C、同温同压下,气体体积相同 |
| D、同温同压下,气体的密度相同 |
2007年诺贝尔化学奖授予德国化学家Gerhard Ertl,以表彰他在固体表面化学研究过程中的重大发现.使CO、NOx等在铂表面发生化学反应转变成无毒气体,以减少汽车尾气中有毒气体的排放,正是此项研究的重要应用之一.下列有关说法不正确的是( )
| A、使用催化剂可以加快反应速率 |
| B、改变压强对反应速率无影响 |
| C、增大压强可加快反应速率 |
| D、升高温度反应速率加快 |
下列说法中正确的是( )
| A、18g水的物质的量是1mol,它在标准状况下的体积约为22.4L |
| B、当温度高于0℃时,气体摩尔体积一定大于22.4L/mol |
| C、22.4L气体所含的分子数一定大于11.2L气体所含的分子数 |
| D、标准状况下,32gO2的体积约为22.4L |
 所示,则苯氯乙酮不可能具有的化学性质是
所示,则苯氯乙酮不可能具有的化学性质是
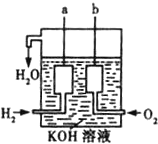 氢气燃烧生成液态水的热化学方程式是2H2(g)+O2(g)═2H2O(l);△H=-572kJ/mol请回答下列问题:
氢气燃烧生成液态水的热化学方程式是2H2(g)+O2(g)═2H2O(l);△H=-572kJ/mol请回答下列问题: