题目内容
19.解释下列事实的方程式不正确的是( )| A. | Al溶于NaOH溶液:2Al+2H2O+2NaOH═2NaAlO2+3H2↑ | |
| B. | 盛放NaOH溶液的试剂瓶不能用玻璃塞:SiO2+2OH-═SiO32-+H2O | |
| C. | 向FeCl3溶液中滴加淀粉碘化钾溶液,溶液变蓝:2Fe3++2I-═2Fe2++I2 | |
| D. | 红热的Fe丝与水接触,表面形成蓝黑色保护层:2Fe+3H2O(g) $\frac{\underline{\;\;△\;\;}}{\;}$ Fe2O3+3H2↑ |
分析 A.反应生成偏铝酸钠和氢气;
B.反应生成硅酸钠和水;
C.发生氧化还原反应,遵循电子、电荷守恒;
D.反应生成四氧化三铁和氢气.
解答 解:A.Al溶于NaOH溶液的化学反应为2Al+2H2O+2NaOH═2NaAlO2+3H2↑,故A正确;
B.盛放NaOH溶液的试剂瓶不能用玻璃塞的离子反应为SiO2+2OH-═SiO32-+H2O,故B正确;
C.向FeCl3溶液中滴加淀粉碘化钾溶液,溶液变蓝的离子反应为2Fe3++2I-═2Fe2++I2,故C正确;
D.红热的Fe丝与水接触,表面形成蓝黑色保护层的化学反应为3Fe+4H2O(g) $\frac{\underline{\;\;△\;\;}}{\;}$ Fe3O4+4H2↑,故D错误;
故选D.
点评 本题考查离子反应及化学反应方程式的书写,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
相关题目
9.在分开盛放的M、N两溶液中,各含下列十四种离子中的七种:Al3+、Na+、K+、Fe3+、NH4+、H+、Cl-、NO3-、OH-、S2-、MnO4-、SO42-、AlO2-、CO32-,且两溶液里所含离子不相同,已知M溶液中的阳离子只有两种,则N溶液中的阴离子应该是( )
| A. | NH4+ S2- CO32- | B. | AlO21 SO42- MnO4- | ||
| C. | NO3- Cl- SO42- | D. | MnO4- SO42- NO3- |
10.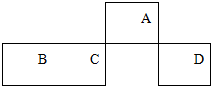 短周期元素A、B、C、D在元素周期表中的相对位置如图所示,其中A的最高价和最低负价的代数和是2.下列判断不正确的是( )
短周期元素A、B、C、D在元素周期表中的相对位置如图所示,其中A的最高价和最低负价的代数和是2.下列判断不正确的是( )
 短周期元素A、B、C、D在元素周期表中的相对位置如图所示,其中A的最高价和最低负价的代数和是2.下列判断不正确的是( )
短周期元素A、B、C、D在元素周期表中的相对位置如图所示,其中A的最高价和最低负价的代数和是2.下列判断不正确的是( )| A. | C元素在地壳中的含量仅次于氧元素 | |
| B. | 最高价氧化物对应水化物的酸性:C<D | |
| C. | 元素A与元素B形成的化合物BA是一种新型无机非金属材料 | |
| D. | 实验室可用B的单质与A元素最高价氧化物对应的水化物反应制取氢气 |
14.不同温度下,水溶液中c(H+)与c(OH-)关系如图所示.下列说法正确的是( )
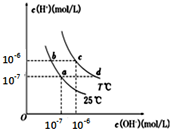

| A. | a点对应的溶液中大量存在:Na+、Mg2+、Cl-、SO42- | |
| B. | b点对应的溶液中大量存在:Fe2+、Ba2+、Cl-、NO3- | |
| C. | c点对应的溶液中大量存在:K+、Al3+、Cl-、CO32- | |
| D. | d点对应的溶液中大量存在:Na+、NH4+、ClO-、Cl- |
11.常温常压下,将NH3缓慢通入饱和食盐水中至饱和,然后向所得溶液中缓慢通入CO2,整个实验过程中溶液的pH随通入气体体积的变化曲线如图所示(实验中不考虑氨水的挥发).下列叙述正确的是( )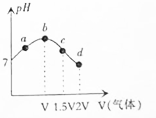

| A. | d点所示溶液中:c(NH4+)+c(NH3•H2O)=c(HCO3-)+c(CO32-)+c(H2CO3) | |
| B. | a点到b点的过程中,溶液中$\frac{c(N{{H}_{4}}^{+})}{c(N{H}_{3}•{H}_{2}O)}$增大 | |
| C. | c点所示溶液中,c(CO32-)>c(NH4+)>c(OH-)>c(H+) | |
| D. | 由图可知(NH4)2CO3溶液显碱性、NH4Cl溶液显酸性 |
8.不用其他试剂鉴别:①NaOH②KCl③Mg(NO3)2④CuSO4四种溶液,先直接鉴别出一种,再逐一鉴别其余物质,则正确的鉴别顺序是( )
| A. | ④①③② | B. | ①④③② | C. | ①③④② | D. | ④②①③ |
9.下列有机反应中,不属于取代反应的是( )
| A. | 乙醇与乙酸的反应 | |
| B. | 蛋白质的水解反应 | |
| C. | 苯和浓硝酸、浓硫酸混合液在50-60℃水浴中发生的反应 | |
| D. | 乙烯使溴水褪色 |
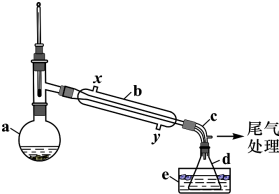
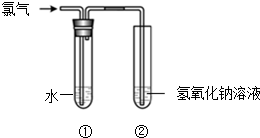 某同学用如图所示装置制取氯水并进行相关实验.
某同学用如图所示装置制取氯水并进行相关实验.