题目内容
某仅由碳、氢、氧三种元素组成的有机化合物,经测定其相对分子质量为90。取有机物样品1.8g,在纯氧中完全燃烧,将产物先后通过浓硫酸和碱石灰,两者分别增重1.08g和2.64g。试求该有机物的分子式。
【答案】
C3H6O3
【解析】
试题分析:浓硫酸吸收的是水
则水的物质的量是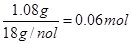
碱石灰吸收的是CO2
则CO2的物质的量是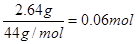
其中碳、氢原子的质量分别是
m(H)=0.06mol×1g/mol=0.12g
m(C)=0.006mol×12g/mol=0.72g
所以根据质量守恒定律可知,有机物中氧原子的质量是
m(O)=1.8g―0.12g―0.72g=0.96g
其物质的量是
所以n(C)∶n(H)∶n(O)=0.06∶0.12∶0.06=1∶2∶1
因此其实验式为CH2O
所以可设其分子式为 (CH2O)n
则有30n=90
解之得n=3
所以分子式为C3H6O3
考点:考查有机物燃烧的有关计算
点评:本题属于高考中的常见题型,为中等难度的试题,试题难易适中。有利于培养学生的规范答题能力,拓展学生的思维方式,提高学生的学习效率,激发学生的求知欲。

练习册系列答案
相关题目