题目内容
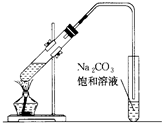 如图是实验室制乙酸乙酯的装置.
如图是实验室制乙酸乙酯的装置.(1)在大试管中配制一定比例的乙醇、乙酸和浓硫酸的混合溶液的方法是将
(2)装置中通蒸气的导管要插在
(3)浓硫酸的作用是①
(4)饱和Na2CO3溶液的作用是
(5)实验生成的乙酸乙酯,其密度比水
(6)若实验中温度过高,使反应温度达到140℃左右时,副反应的主要有机产物是
考点:乙酸乙酯的制取
专题:实验题
分析:(1)为防止酸液飞溅,应将密度大的液体加入到密度小的液体中,即将浓H2SO4慢慢倒人乙醇和乙酸的混合液中;
(2)防止由于加热不均匀造成Na2CO3溶液倒流进加热反应物的试管中,导致试管破裂;
(3)乙酸与乙醇在浓硫酸作催化剂加热条件下生成乙酸乙酯,由于反应为可逆反应,同时浓硫酸吸水有利于平衡向生成乙酸乙酯的方向移动;
(4)实验室里用饱和碳酸钠溶液冷却乙酸乙酯的原因:除去乙酸和乙醇,并降低乙酸乙酯的溶解度,增大水的密度,使酯浮于水面,容易分层析出,便于分离;
(5)乙酸与乙醇在浓硫酸作用下加热发生酯化反应生成乙酸乙酯,酯类的密度比水小,低级酯有香味;
(6)乙醇在浓硫酸作用下加热到在140℃发生分子间脱水生成乙醚.
(2)防止由于加热不均匀造成Na2CO3溶液倒流进加热反应物的试管中,导致试管破裂;
(3)乙酸与乙醇在浓硫酸作催化剂加热条件下生成乙酸乙酯,由于反应为可逆反应,同时浓硫酸吸水有利于平衡向生成乙酸乙酯的方向移动;
(4)实验室里用饱和碳酸钠溶液冷却乙酸乙酯的原因:除去乙酸和乙醇,并降低乙酸乙酯的溶解度,增大水的密度,使酯浮于水面,容易分层析出,便于分离;
(5)乙酸与乙醇在浓硫酸作用下加热发生酯化反应生成乙酸乙酯,酯类的密度比水小,低级酯有香味;
(6)乙醇在浓硫酸作用下加热到在140℃发生分子间脱水生成乙醚.
解答:
解:(1)为防止液体飞溅,原理和浓H2SO4加入水中相同,方法为:将浓H2SO4慢慢倒人乙醇和乙酸的混合液中,然后轻轻地振荡试管,使之混合均匀,
故答案为:浓H2SO4慢慢倒人乙醇和乙酸的混合液中;
(2)加热不均匀易造成Na2CO3溶液倒流进加热反应物的试管中,导致试管破裂,
故答案为:饱和Na2CO3溶液的液面上方,不能插入溶液中;防止Na2CO3溶液的倒吸;
(3)乙酸与乙醇在浓硫酸作催化剂加热条件下生成乙酸乙酯,由于反应为可逆反应,同时浓硫酸吸水有利于平衡向生成乙酸乙酯的方向移动,
故答案为:催化剂;吸水剂;
(4)制备乙酸乙酯时常用饱和碳酸钠溶液吸收乙酸乙酯,主要是利用了乙酸乙酯难溶于饱和碳酸钠,乙醇与水混溶,乙酸能被碳酸钠吸收,易于除去杂质,
故答案为:溶解乙醇、中和乙酸;降低乙酸乙酯的溶解度,便于分层析出;
(5)乙酸与乙醇在浓硫酸作用下加热发生酯化反应生成乙酸乙酯和水:CH3COOH+C2H5OH CH3COOC2H5+H2O,生成的乙酸乙酯的密度小于水的密度,有果香气味,
CH3COOC2H5+H2O,生成的乙酸乙酯的密度小于水的密度,有果香气味,
故答案为:小;果香;
(6)乙醇在140℃,在浓硫酸催化下脱水生成乙醚,结构简式为:CH3CH2OCH2CH3,
故答案为:乙醚 CH3CH2OCH2CH3.
故答案为:浓H2SO4慢慢倒人乙醇和乙酸的混合液中;
(2)加热不均匀易造成Na2CO3溶液倒流进加热反应物的试管中,导致试管破裂,
故答案为:饱和Na2CO3溶液的液面上方,不能插入溶液中;防止Na2CO3溶液的倒吸;
(3)乙酸与乙醇在浓硫酸作催化剂加热条件下生成乙酸乙酯,由于反应为可逆反应,同时浓硫酸吸水有利于平衡向生成乙酸乙酯的方向移动,
故答案为:催化剂;吸水剂;
(4)制备乙酸乙酯时常用饱和碳酸钠溶液吸收乙酸乙酯,主要是利用了乙酸乙酯难溶于饱和碳酸钠,乙醇与水混溶,乙酸能被碳酸钠吸收,易于除去杂质,
故答案为:溶解乙醇、中和乙酸;降低乙酸乙酯的溶解度,便于分层析出;
(5)乙酸与乙醇在浓硫酸作用下加热发生酯化反应生成乙酸乙酯和水:CH3COOH+C2H5OH
 CH3COOC2H5+H2O,生成的乙酸乙酯的密度小于水的密度,有果香气味,
CH3COOC2H5+H2O,生成的乙酸乙酯的密度小于水的密度,有果香气味,故答案为:小;果香;
(6)乙醇在140℃,在浓硫酸催化下脱水生成乙醚,结构简式为:CH3CH2OCH2CH3,
故答案为:乙醚 CH3CH2OCH2CH3.
点评:本题考查了乙酸乙酯的反应原理及制备方法,题目难度中等,注意掌握乙酸乙酯的反应原理及实验室制法,明确浓硫酸、饱和碳酸钠溶液的作用及制取混合酸的正确方法为解答本题的关键.

练习册系列答案
相关题目
已知氧化性Br2>Fe3+.FeBr2溶液中通入一定量的Cl2,发生反应的离子方程式为:aFe2++bBr-+cCl2═dFe3++eBr2+fCl-下列选项中的数字与离子方程式中的a、b、c、d、e、f一一对应,其中不符合反应实际的是( )
| A、2 6 4 2 3 8 |
| B、2 4 3 2 2 6 |
| C、2 0 1 2 0 2 |
| D、2 2 2 2 1 4 |
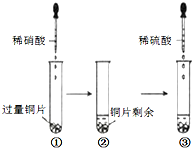 某实验过程如图所示,则图③试管中的现象是( )
某实验过程如图所示,则图③试管中的现象是( )| A、铜片溶解,产生无色气体,该气体遇空气变为红棕色 |
| B、铜片溶解,产生无色气体,该气体遇到空气不变色 |
| C、铜片溶解,放出红棕色有刺激性气味的气体 |
| D、无明显现象,因稀硫酸不与铜反应 |
下列实验操作能达到目的是( )
| A、除去乙醛中的乙酸杂质:加入氢氧化钠溶液洗涤,分液 |
| B、检验乙醇中是否含水:用无水硫酸铜,观察是否变蓝色 |
| C、鉴别SO2和Cl2:通入品红溶液,观察是否褪色 |
| D、获得NH4Cl晶体:将NH4Cl溶液蒸发浓缩,冷却结晶,过滤 |
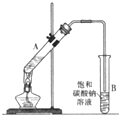 乙酸乙酯是重要的化工原料.实验室合成乙酸乙酯的装置如图所示.
乙酸乙酯是重要的化工原料.实验室合成乙酸乙酯的装置如图所示.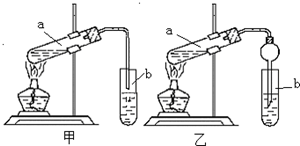 某实验小组欲制取乙酸乙酯,设计了如下图所示的装置,请回答有关问题:
某实验小组欲制取乙酸乙酯,设计了如下图所示的装置,请回答有关问题: 有X、Y、Z、M、G五种元素,是分属三个短周期并且原子序数依次增大的主族元素.其中X、Z同主族,可形成离子化合物ZX;Y、M同主族,可形成MY2、MY3两种分子.完成下列填空:
有X、Y、Z、M、G五种元素,是分属三个短周期并且原子序数依次增大的主族元素.其中X、Z同主族,可形成离子化合物ZX;Y、M同主族,可形成MY2、MY3两种分子.完成下列填空: