题目内容
将标准状况下的aL HCl(g)溶于1000g水中,得到的盐酸密度为b g·cm-3,则该盐酸的物质的量浓度是
A.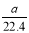 mo1·L-1 B.
mo1·L-1 B.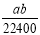 mol·L-1
mol·L-1
C.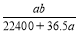 mol·L-1 D.
mol·L-1 D.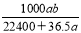 mol·L-1
mol·L-1
D
【解析】
试题分析:m(HCl)=(aL÷22.4L/mol)×36.5g/mol;m(溶液)=m(溶质)+m(溶剂)= (aL÷22.4L/mol)×36.5g/mol+1000g,溶质的质量分数是ω= m(溶质)÷m(溶液)= [(aL÷22.4L/mol)×36.5g/mol]÷(aL÷22.4L/mol)×36.5g/mol+1000g,所以溶液的物质的量浓度c= =
= mol/L,所以选项是D。
mol/L,所以选项是D。
考点:考查溶液的质量发生与物质的量浓度的换算和计算的知识。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
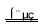 2OH- +Cl2↑ +H2↑
2OH- +Cl2↑ +H2↑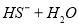
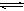
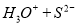
 PCl 3(g)+Cl2(g) ① 2HI(g)
PCl 3(g)+Cl2(g) ① 2HI(g)