题目内容
12.常温下,有关 0.1mol/LCH3COONa 溶液(pH>7),下列说法不正确的是( )| A. | 根据以上信息,可推断CH3COOH为弱电解质 | |
| B. | 加水稀释过程中,c(H+)•c(OH-) 的值增大 | |
| C. | 加入NaOH固体可抑制 CHCOO-的水解 | |
| D. | 同pH的CH3COONa溶液和NaOH溶液,由水电离出的c(H+) 前者大 |
分析 A.CH3COONa溶液显碱性,可说明为强碱弱酸盐,可证明醋酸为弱酸;
B.溶液中离子积常数随温度变化;
C.醋酸钠溶液中醋酸根离子水解溶液显碱性,加入氢氧化钠抑制水解;
D.水解的盐促进水的电离,氢氧化钠是强碱溶液抑制水的电离.
解答 解:A.0.1mol/LCH3COONa 溶液pH>7,溶液显碱性说明醋酸根离子水解,醋酸钠为强碱弱酸盐,可证明醋酸为弱酸,故A正确;
B.常温下,有关 0.1mol/LCH3COONa 溶液,加水稀释促进水解,但溶液中离子积常数c(H+)•c(OH-) 的值不变,故B错误;
C.醋酸钠溶液中醋酸根离子水解,溶液显碱性,CH3COO-+H2O?CH3COOH+OH-,加入NaOH固体可抑制 CH3COO-的水解,故C正确;
D.同pH的CH3COONa溶液和NaOH溶液,醋酸钠水解促进水的电离,氢氧化钠溶液抑制谁的电离,由水电离出的c(H+) 前者大,故D正确;
故选B.
点评 本题考查了弱电解质的判断、盐类水解原理分析、影响水电离的因素判断等知识点,明确弱电解质的性质和离子积常数随温度变化是解答本题的关键,题目难度中等.

练习册系列答案
相关题目
2.填写如表
(1)
(2)画出下列粒子的结构示意图:S2-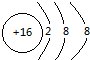 Mg2+
Mg2+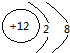 .
.
(1)
| 微粒符号 | 质子数 | 中子数 | 电子数 | 质量数 | |
| ① | ${\;}_{19}^{40}$K | 19 | 21 | 19 | 40 |
| ② | 3818Ar | 18 | 20 | 18 | 38 |
| ③ | 3216S2- | 16 | 16 | 18 | 32 |
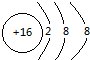 Mg2+
Mg2+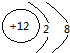 .
.
3.NA为阿伏伽德罗常数,下列说法错误的是( )
| A. | 1molNa与O2反应得到32g固体产物,钠失去电子数为NA | |
| B. | 用1mL0.1mol•L-1FeCl3溶液制得的氢氧化铁胶体所含胶粒数为10-4NA | |
| C. | 12g金刚石中含有的共价键数为2NA | |
| D. | 标准状况下,22.4LCH4中含有的碳原子数为NA |
20. 含乙酸钠和对氯酚(
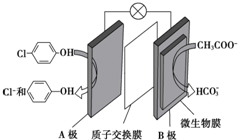
含乙酸钠和对氯酚(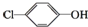 )的废水可以利用微生物电池除去,其原理如图所示,下列有关说法不正确的是( )
)的废水可以利用微生物电池除去,其原理如图所示,下列有关说法不正确的是( )
 含乙酸钠和对氯酚(
含乙酸钠和对氯酚( )的废水可以利用微生物电池除去,其原理如图所示,下列有关说法不正确的是( )
)的废水可以利用微生物电池除去,其原理如图所示,下列有关说法不正确的是( )| A. | 电极B是负极 | |
| B. | 质子从A极移向B极 | |
| C. | B极的电极反应式:CH3COO--8e-+4H2O═2HCO3-+9H+ | |
| D. | 处理后的废水pH降低 |
7.如表为元素周期表的一部分,X、Y、Z、W 为短周期元素,其中
Z 元素的原子最外层电子数是其核电荷数的$\frac{3}{4}$.下列说法不正确的是( )
| X | Y | Z |
| W | ||
| T |
| A. | Y、W、T元素的原子半径及它们气态氢化物的还原性均依次递增 | |
| B. | Z氢化物的沸点一定比 X氢化物的沸点高 | |
| C. | X、Y元素形成的常见单质的化学键类型相同 | |
| D. | 根据元素周期律,可以推测存在化学式为T2Z3、X3Y4的两种物质,T元素存在同素异形现象 |
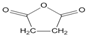 ),试剂③是环氧乙烷(
),试剂③是环氧乙烷(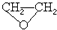 ),且环氧乙烷在酸或碱中易水解或聚合.
),且环氧乙烷在酸或碱中易水解或聚合.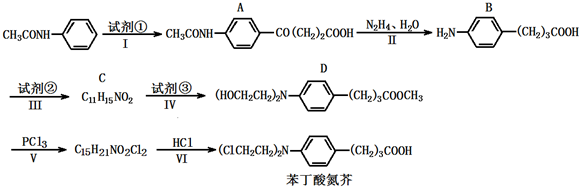
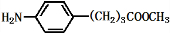
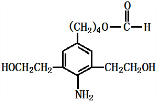
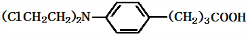 +3NaOH$\stackrel{△}{→}$
+3NaOH$\stackrel{△}{→}$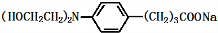 +2NaCl+H2O
+2NaCl+H2O
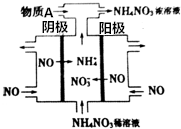 如图是利用N2H4-KOH-O2为电源点解NO制备NH4NO3,其工作原理如图所示:
如图是利用N2H4-KOH-O2为电源点解NO制备NH4NO3,其工作原理如图所示: