题目内容
10.用NaOH与Na2CO3•nH2O的混合物共有28g配制成100mL溶液,测得该溶液中c(Na+)=4mol•L-1,另取相同质量的上述混合物,加入足量的盐酸完全反应后,放出的气体在标准状况下的体积为3.36L,试计算:(1)原混合物中NaOH的质量分数;
(2)Na2CO3•nH2O中的n值.
分析 (1)发生反应:NaOH+HCl═NaCl+H2O、Na2CO3+2HCl═2NaCl+CO2↑+H2O,根据碳原子守恒可知n(Na2CO3•nH2O)=n(Na2CO3)=n(CO2),根据Na+守恒计算n(NaOH),进而计算NaOH 的质量分数;
(2)计算Na2CO3•nH2O的摩尔质量,进而计算n值.
解答 解:有关化学方程式:NaOH+HCl=NaCl+H2O、Na2CO3+2HCl=2NaCl+CO2↑+H2O,
(1)根据碳原子守恒:n(Na2CO3•nH2O)=n(Na2CO3)=n(CO2)=$\frac{3.36L}{22.4mol•L}$=0.15mol,
根据Na+守恒,有n(NaOH)=0.1L×4mol/L-0.15mol×2=0.1mol,
所以m(NaOH)%═$\frac{0.1mol×40gmo{l}^{-1}}{28g}$×100%=14.3%,
答:原混合物中NaOH 的质量分数为14.3%;
(2)M(Na2CO3•nH2O)=$\frac{28g-4g}{0.15mol}$=160g/mol,所以:n=$\frac{160-106}{18}$=3,
答:Na2CO3•nH2O 中的n=3.
点评 本题考查混合物计算,难度中等,注意利用守恒法进行计算,侧重对学生思维能力的考查.

练习册系列答案
 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案
相关题目
1.我国西部地区有丰富的盐湖资源,对盐湖矿产资源的综合开发利用是西部大开发的重要课题之一.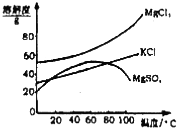
I.某研究性学习小组拟取盐湖苦卤的浓缩液(富含K+、Mg2+、Br-、SO42-、Cl-等),来制取较纯净的氯化钾晶体及液溴,他们设计了如下流程:
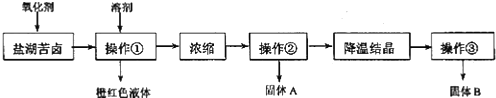
II.某同学提出了另一种新方案,对上述操作①后无色溶液进行除杂提纯,无色溶液中先 加试剂 A,再加试剂 B,最后加试剂 C(常见的盐),其方案如下:
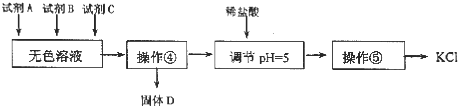
下列说法不正确的是( )

I.某研究性学习小组拟取盐湖苦卤的浓缩液(富含K+、Mg2+、Br-、SO42-、Cl-等),来制取较纯净的氯化钾晶体及液溴,他们设计了如下流程:

II.某同学提出了另一种新方案,对上述操作①后无色溶液进行除杂提纯,无色溶液中先 加试剂 A,再加试剂 B,最后加试剂 C(常见的盐),其方案如下:

下列说法不正确的是( )
| A. | 要从橙红色液体中分离出单质溴,可采取的操作是蒸馏 | |
| B. | 操作②为过滤,主要目的是为了除去 MgSO4 | |
| C. | 试剂 C为K2CO3,固体D主要为Mg(OH)2、BaSO4,还有少量的BaCO3 | |
| D. | 若在操作④结束后发现溶液略有浑浊,应采取的措施是更换滤纸,重新过滤 |
5.有机物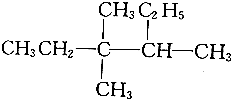 的准确命名是( )
的准确命名是( )
 的准确命名是( )
的准确命名是( )| A. | 3,3二甲基-4-乙基戊烷 | B. | 3,3,4-三甲基已烷 | ||
| C. | 3,3,4,-三甲基已烷 | D. | 2,3,3-三甲基已烷 |
2.下列各组混合物,使用氢氧化钠溶液和盐酸两种试剂不能分离的是( )
| A. | 氧化镁中混有氧化铝 | B. | 氯化铝溶液中混有氯化铁 | ||
| C. | 氧化铁中混有二氧化硅 | D. | 氯化亚铁溶液中混有氯化铜 |
2.在呼吸面具和潜水艇中可用过氧化钠作为供氧剂.请选用适当的化学试剂和实验用品,用如图中的实验装置进行实验,证明过氧化钠可作供氧剂.
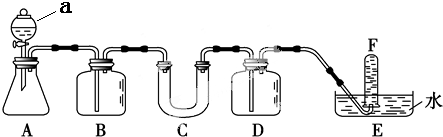
(1)写出仪器a的名称分液漏斗.
(2)A是实验室制取CO2的装置.写出A中发生反应的离子方程式:CaCO3+2H+═CO2↑+H2O+Ca2+.
(3)填写表中空格:
(4)写出仪器C中主要反应的化学方程式:2Na2O2+2CO2=2Na2CO3+O2.
(5)若将钠和过氧化钠的混合物12.4g与足量的水反应后,生成的气体在电火花用下恰好完全反应,且所得溶液的体积为100mL,则所得溶液的物质的量浓度是4mol•L-1.

(1)写出仪器a的名称分液漏斗.
(2)A是实验室制取CO2的装置.写出A中发生反应的离子方程式:CaCO3+2H+═CO2↑+H2O+Ca2+.
(3)填写表中空格:
| 仪器 | 加入试剂 | 加入该试剂的目的 |
| B | 饱和碳酸氢钠溶液 | |
| D |
(5)若将钠和过氧化钠的混合物12.4g与足量的水反应后,生成的气体在电火花用下恰好完全反应,且所得溶液的体积为100mL,则所得溶液的物质的量浓度是4mol•L-1.
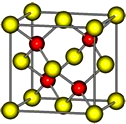 有A、B、C、D、E五种前四周期的元素.A原子核外有1个未成对电子,A+比B原子少一个电子层,B原子得一个电子填入3p轨道后,3p轨道呈全充满状态.C原子的2p轨道有2个未成对电子,D的最高化合价和最低化合价的代数和为4,与C的核电荷数相差8.E位于周期表第12纵列且是六种元素中原子序数最大的.R是由D、E形成的化合物,其晶胞结构如图所示.请回答下列问题:
有A、B、C、D、E五种前四周期的元素.A原子核外有1个未成对电子,A+比B原子少一个电子层,B原子得一个电子填入3p轨道后,3p轨道呈全充满状态.C原子的2p轨道有2个未成对电子,D的最高化合价和最低化合价的代数和为4,与C的核电荷数相差8.E位于周期表第12纵列且是六种元素中原子序数最大的.R是由D、E形成的化合物,其晶胞结构如图所示.请回答下列问题: .
.
 .
. .
.