题目内容
使Cl2和H2O(g)通过灼热的炭层,生成HCl和CO2,是放热反应,当1mol Cl2参与反应时释放145kJ的热量,写出这个反应的热化学方程式: .
考点:有关反应热的计算
专题:
分析:反应热与反应计量数呈正比,1mol Cl2参与反应时释放145kJ的热量,2mol Cl2参与反应时释放290kJ的热量,依据热化学方程式书写方法写出,标注物质聚集状态和对应焓变.
解答:
解:使Cl2和H2O(g)通过灼热的炭层,生成HCl和CO2是放热反应,当1mol Cl2参与反应时释放145kJ的热量,2mol氯气完全反应放热290 kJ,热化学方程式为2Cl2(g)+2H2O(g)+C(s)═4HCl(g)+CO2(g)△H=-290 kJ?mol-1,
故答案为:2Cl2(g)+2H2O(g)+C(s)═4HCl(g)+CO2(g)△H=-290 kJ?mol-1.
故答案为:2Cl2(g)+2H2O(g)+C(s)═4HCl(g)+CO2(g)△H=-290 kJ?mol-1.
点评:本题考查反应热的计算,侧重于学生的计算能力和分析能力的考查,注意反应热与计量数的关系,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列说法正确的是( )
| A、硅元素主要以单质、氧化物、硅酸盐的形式存在于自然界中 |
| B、浓氨水中滴加FeCl3饱和溶液可制得Fe(OH)3胶体 |
| C、用饱和食盐水替代水跟电石反应,可以减缓乙炔的产生速率 |
| D、Ca(HCO3)2溶液与过量NaOH溶液反应可制得Ca(OH)2 |
下列过程不涉及氧化还原反应的是( )
| A、二氧化氮气体冷却后颜色变浅 |
| B、镁条在二氧化碳气体中燃烧 |
| C、人工固氮 |
| D、久置的浓硝酸显黄色 |
将25%的硫酸溶液和5%的硫酸溶液等体积混合,所得硫酸溶液的质量分数是( )
| A、等于15% | B、大于15% |
| C、小于15% | D、无法估算 |
标准状况下,将V L A气体(摩尔质量为Mg/mol)溶于0.1L水(密度1g/cm3)中,所得溶液的密度为dg/mL,则此溶液的物质的量浓度(mol/L)为( )
A、
| ||
B、
| ||
C、
| ||
D、
|
下列做法体现了环境保护理念的有( )
| A、大力推广使用含甲醛涂料 |
| B、研究开发可降解塑料 |
| C、燃烧废旧电线提取铜线 |
| D、将实验室废液集中进行无害化处理 |
下列物质中含分子数目最多的是( )
| A、0.1mol Cl2 |
| B、0.4g H2 |
| C、4℃时9mLH2O |
| D、标况下,6.72L CO2 |
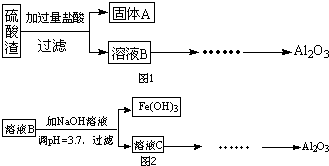 (1)写出溶液B的溶质是
(1)写出溶液B的溶质是