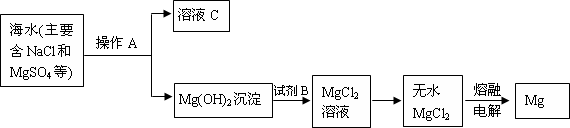
题目内容
某化学研究小组的同学为比较Fe3+和Cu2+对H2O2分解的催化效果,分别设计了如图甲、乙所示的实验.请回答相关问题:
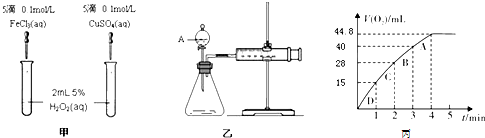
(1)定性分析:根据甲中观察到的 现象,可定性比较得出结论.有同学提出用FeCl3不妥,改为Fe2(SO4)3更为合理,其理由是 .
(2)定量分析:如图乙所示,图中仪器A的名称为 ,检查该装置气密性的方法是 .若实验中均得到标况下VmL气体,要计算速率还需要测量的数据是 .
(3)取0.5g MnO2粉末加入12.50mL H2O2溶液中,放出气体(标况下)的体积和时间的关系如图丙所示.则从反应开始到2min末,v(H2O2)= ,此时H2O2的分解率为 .(设溶液体积不变且最后双氧水完全分解)

(1)定性分析:根据甲中观察到的
(2)定量分析:如图乙所示,图中仪器A的名称为
(3)取0.5g MnO2粉末加入12.50mL H2O2溶液中,放出气体(标况下)的体积和时间的关系如图丙所示.则从反应开始到2min末,v(H2O2)=
考点:浓度、温度、催化剂对化学反应速率的影响
专题:化学反应速率专题
分析:(1)根据反应生成气体的快慢分析;根据H2O2分解的催化作用有可能是氯离子起的作用,改为Fe2(SO4)3使阳离子相同,更为合理;根据反应物、生成物、反应条件写出反应方程式;
(2)依据常见仪器填空;根据乙图装置来选择气密性的检查方法;该反应是通过反应速率分析的,所以根据v=
来判断;
(3)依据2min内生成氧气的体积计算氧气的化学反应速率,再依据化学反应方程式化学计量数之比计算双氧水的速率,最后依据氧气生成总体积与2min时体积,计算转化率即可.
(2)依据常见仪器填空;根据乙图装置来选择气密性的检查方法;该反应是通过反应速率分析的,所以根据v=
| △c |
| △t |
(3)依据2min内生成氧气的体积计算氧气的化学反应速率,再依据化学反应方程式化学计量数之比计算双氧水的速率,最后依据氧气生成总体积与2min时体积,计算转化率即可.
解答:
解:(1)该反应中产生气体,而且反应放热,所以可根据反应产生气泡快慢或反应完成的先后或试管壁的冷热程度来判断;H2O2分解的催化作用有可能是氯离子起的作用,改为Fe2(SO4)3使阳离子相同,这样可以控制阴离子相同,排除阴离子的干扰,更为合理,
故答案为:反应产生气泡快慢或反应完成的先后或试管壁的冷热程度;控制阳离子相同,排除阳离子的干扰;
(2)结合乙图装置,仪器A为分液漏斗,该气密性的检查方法为:关闭分液漏斗活塞,将注射器活塞拉出一定距离,一段时间后松开活塞,观察活塞是否回到原位;反应是通过反应速率分析的,根据v=
,所以,实验中需要测量的数据是时间(或收集一定体积的气体所需要的时间).
故答案为:分液漏斗;关闭分液漏斗活塞,将注射器活塞拉出一定距离,一段时间后松开活塞,观察活塞是否回到原位;时间(或收集一定体积的气体所需要的时间);
(3)2H2O2
2H2O+O2↑,从反应开始到2min,生成氧气的体积为28mL,故氧气的物质的量为:
,故v(O2)=
=
mol/(L?min),故v(H2O2)=2×
=
=1.25×10-3mol/(L?min),依据题目可知,双氧水完全分解生成氧气的体积为44.8mL,故2min时,双氧水的分解率为:
×100%=62.5%,故答案为:1.25×10-3mol/(L?min);62.5%.
故答案为:反应产生气泡快慢或反应完成的先后或试管壁的冷热程度;控制阳离子相同,排除阳离子的干扰;
(2)结合乙图装置,仪器A为分液漏斗,该气密性的检查方法为:关闭分液漏斗活塞,将注射器活塞拉出一定距离,一段时间后松开活塞,观察活塞是否回到原位;反应是通过反应速率分析的,根据v=
| △c |
| △t |
故答案为:分液漏斗;关闭分液漏斗活塞,将注射器活塞拉出一定距离,一段时间后松开活塞,观察活塞是否回到原位;时间(或收集一定体积的气体所需要的时间);
(3)2H2O2
| ||
| 28×10-3L |
| 22.4L/mol |
| ||
| 2 |
| 28×10-3 |
| 44.8 |
| 28×10-3 |
| 44.8 |
| 28×10-3 |
| 22.4 |
| 28mL |
| 44.8mL |
点评:本题主要考查了催化剂的作用及化学反应速率的影响因素等知识点,难度不大,要会分析将FeCl3改为Fe2(SO4)3更为合理的理由.

练习册系列答案
相关题目
镧系元素的水合氯化物LnCl3?nH2O,加热脱水时易发生分解,为了制无水LnCl3,可采用的措施是( )
| A、在HCl气流中加热使之脱水 |
| B、在NH3气流中加热使之脱水 |
| C、加入P2O5固体加热使之脱水 |
| D、加入H2SO4加热使之脱水 |
下面关于Na2CO3和NaHCO3性质的叙述,不正确的是( )
| A、在水中的溶解度:碳酸钠>碳酸氢钠 |
| B、热稳定性:碳酸钠>碳酸氢钠 |
| C、溶液酸碱性:物质的量浓度相同时,Na2CO3溶液pH小于NaHCO3溶液的pH |
| D、等质量的碳酸钠和碳酸氢钠分别与足量的盐酸反应,消耗HCl的量前者多 |
甲酸溶液中存在电离平衡HCOOH?H++HCOO-,下列叙述不正确的是( )
| A、醋酸溶液中离子浓度的关系满足:c(H+)=c(OH-)+c(HCOO-) |
| B、0.01mol/L的HCOOH溶液中加水稀释,溶液中c(OH-)减小 |
| C、HCOOH溶液中加少量的HCOONa固体,平衡逆向移动 |
| D、常温下pH=2的HCOOH溶液与pH=12的NaOH溶液等体积混合后,pH<7 |