题目内容
等质量的两种气体SO2和SO3,其物质的量之比为 ,二者所含O原子个数之比为 ,在同温同压下的体积之比为 .
考点:物质的量的相关计算
专题:计算题
分析:n=
、V=nVm、N=nNA,并结合物质的构成来解答.
| m |
| M |
解答:
解:等质量的两种气体SO2和SO3,其物质的量之比为
:
=5:4,
含O原子个数比等于含O原子的物质的量之比,即为5×2:4×3=5:6,
同温同压下,Vm相同,体积之比等于物质的量之比,即为5:4,
故答案为:5:4;5:6;5:4.
| m |
| 64 |
| m |
| 80 |
含O原子个数比等于含O原子的物质的量之比,即为5×2:4×3=5:6,
同温同压下,Vm相同,体积之比等于物质的量之比,即为5:4,
故答案为:5:4;5:6;5:4.
点评:本题考查物质的量的有关计算,为高频考点,把握质量、体积、物质的量的关系为解答的关键,侧重基本公式及计算能力的考查,题目难度不大.

练习册系列答案
相关题目
全钒液流储能电池是利用不同价态离子对的氧化还原反应来实现化学能和电能相互转化的装置,其原理如图所示.下列说法错误的是( )


| A、当左槽溶液逐渐由黄变蓝,其电极反应式为:VO2++2H++e-=VO2++H2O |
| B、充电过程中,右槽溶液颜色逐渐由绿色变为紫色 |
| C、放电过程中氢离子通过交换膜定向移入左槽 |
| D、充电时若转移的电子数为3.01×1023个,左槽溶液中n(H+)的变化量为1 mol |
以石墨做电极,电解1mol/L下列物质的水溶液,下列表述正确的是( )
| A、若为盐酸溶液,pH减小 |
| B、若为氢氧化钠溶液,pH减小 |
| C、若为硫酸钠溶液,pH不变 |
| D、若为氯化钠溶液,pH不变 |
某固体A在一定条件下加热分解,产物全是气体,A的分解反应为:2A
B↑+2C↑+2D↑,现测得分解产生的混合气体对氢气的相对密度为d,则A的相对分子质量为( )
| ||
| A、2d | B、10d |
| C、5d | D、0.8d |
废电池必须进行集中处理的主要原因是( )
| A、利用电池外壳的金属材料 |
| B、防止电池中汞、镉和铅等重金属离子对土壤和水源的污染 |
| C、防止电池中渗泄的电解液腐蚀其他物品 |
| D、回收其中的石墨电极 |
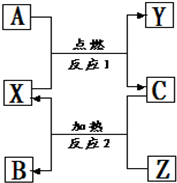 A、B、C是中学化学常见的单质,X、Y、Z是中学化学常见的氧化物,它们之间有如右图所示的转化关系,请据图回答:
A、B、C是中学化学常见的单质,X、Y、Z是中学化学常见的氧化物,它们之间有如右图所示的转化关系,请据图回答: