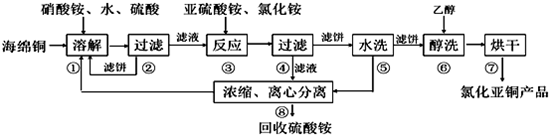
题目内容
3.碱式硫酸铁[Fe(OH)SO4]是一种用于污水处理的新型高效絮凝剂,在医药上也可用于治疗消化性溃疡出血.工业上利用废铁屑(含少量氧化铝、氧化铁等)生产碱式硫酸铁的工艺流程如下: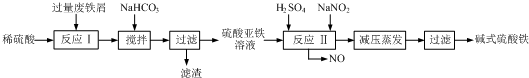
已知:部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 |
| 开始沉淀 | 2.3 | 7.5 | 3.4 |
| 完全沉淀 | 3.2 | 9.7 | 4.4 |
(1)加入少量NaHCO3的目的是调节pH,使溶液中的Al3+沉淀,该工艺中“搅拌”的作用是加快反应速率.
(2)在实际生产中,反应Ⅱ常同时通入O2以减少NaNO2的用量,O2与NaNO2在反应中均作氧化剂.若参与反应的O2有11.2L(标准状况),则相当于节约NaNO2的物质的量为2mol.
(3)碱式硫酸铁溶于水后产生的Fe(OH)2+离子,可部分水解生成Fe2(OH)42+聚合离子.该水解反应的离子方程式为2Fe(OH)2++2H2O?Fe2(OH)42++2H+.
(4)在医药上常用硫酸亚铁与硫酸、硝酸的混合液反应制备碱式硫酸铁.根据我国质量标准,产品中不得含有Fe2+及NO3-.为检验所得产品中是否含有Fe2+,应使用的试剂为D.
A.氯水 B.KSCN溶液 C.NaOH溶液 D.酸性KMnO4溶液.
分析 废铁屑中含少量氧化铝、氧化铁等,将过量废铁屑加入稀硫酸中,发生反应 Fe+H2SO4=FeSO4+H2↑、Al2O3+3H2SO4=Al2(SO4)3+3H2O、Fe2O3+3H2SO4=Fe2(SO4)3+3H2O、Fe2(SO4)3+Fe=3FeSO4,然后反应I中加入NaHCO3并搅拌,调节溶液的pH,发生反应Al3++3HCO3-=Al(OH)3↓+3CO2↑,所以滤渣中成分是Al(OH)3,过滤得到硫酸亚铁,向硫酸亚铁溶液中加入稀硫酸和NaNO2,酸性条件下,NaNO2和FeSO4发生氧化还原反应生成铁离子、NO,将溶液蒸发浓缩、过滤得到碱式硫酸铁,据此分析解答.
解答 解:废铁屑中含少量氧化铝、氧化铁等,将过量废铁屑加入稀硫酸中,发生反应 Fe+H2SO4=FeSO4+H2↑、Al2O3+3H2SO4=Al2(SO4)3+3H2O、Fe2O3+3H2SO4=Fe2(SO4)3+3H2O、Fe2(SO4)3+Fe=3FeSO4,然后反应I中加入NaHCO3并搅拌,调节溶液的pH,发生反应Al3++3HCO3-=Al(OH)3↓+3CO2↑,所以滤渣中成分是Al(OH)3,过滤得到硫酸亚铁,向硫酸亚铁溶液中加入稀硫酸和NaNO2,酸性条件下,NaNO2和FeSO4发生氧化还原反应生成铁离子、NO,将溶液蒸发浓缩、过滤得到碱式硫酸铁,
(1)加入少量NaHCO3的目的是调节pH,根据氢氧化物沉淀需要的pH知,在pH在4.4-7.5之间将Al3+转化为Al(OH)3沉淀,而亚铁离子不能生成沉淀;搅拌的目的是使反应物充分接触反应,从而加快反应速率,
故答案为:Al3+;加快反应速率;
(2)酸性条件下,亚硝酸钠具有氧化性,能将亚铁离子氧化为铁离子,自身被还原生成NO,所以反应Ⅱ中加入NaNO2的目的是氧化Fe2+,发生反应的离子方程式为 2H++Fe2++NO2-=Fe3++NO↑+H2O,氧气的作用与亚硝酸钠相同,1mol氧气得4mol电子,1mol亚硝酸根离子的1mol电子,有$\frac{11.2L}{22.4L/mol}$=0.5mol氧气反应转移2mol电子,相对于2mol亚硝酸钠反应,
故答案为:氧化剂;2mol;
(3)碱式硫酸铁溶于水后产生的Fe(OH)2+离子,Fe(OH)2+可部分水解生成Fe2(OH)42+聚合离子,该水解反应的离子方程式为 2Fe(OH)2++2H2O?Fe2(OH)42++2H+,
故答案为:2Fe(OH)2++2H2O?Fe2(OH)42++2H+;
(4)亚铁离子具有还原性,能被强氧化剂氧化生成铁离子,反应过程中颜色变化明显的效果最佳,
A.氯水为浅黄绿色,氯将亚铁离子氧化为铁离子,溶液呈黄色,颜色变化不明显,故A不选;
B.KSCN溶液和亚铁离子不反应,没有颜色变化,故B不选;
C.NaOH溶液和亚铁离子反应生成白色沉淀,铁离子和氢氧根离子反应生成红褐色沉淀,掩盖氢氧化亚铁颜色,故C不选;
D.酸性KMnO4溶液呈紫色,亚铁离子能被酸性高锰酸钾溶液氧化而使酸性高锰酸钾溶液褪色,现象明显,故D选;
故答案为:D.
点评 本题考查物质的分离和提纯方法的综合应用,题目难度中等,明确实验目的、实验原理为解答关键,试题侧重考查学生获取信息及利用信息能力、分析能力、实验操作能力,注意题给信息的灵活运用,知道常见离子的检验方法及现象.

| A. | 71g氯气含有的原子数目为NA | |
| B. | 4 g金属钙变成钙离子时失去的电子数目为0.1NA | |
| C. | 标准状况下,22.4LH2O中含有的分子数为NA | |
| D. | 在标准状况下,22.4 L甲烷与乙炔的混合物所含分子数为NA |
| 选项 | 正极 | 负极 | 电解质溶液 |
| A | Cu | Zn | 稀盐酸 |
| B | C | Zn | 硫酸铜溶液 |
| C | Cu | Zn | 氯化铜溶液 |
| D | Cu | Zn | 硝酸铜溶液 |
| A. | A | B. | B | C. | C | D. | D |
| A. | v(A)=0.3mol/(L•s) | B. | v(B)=0.6mol/(L•s) | C. | v(C)=0.4mol/(L•s) | D. | v(D)=0.45mol/(L•s) |
| A. | CH3CH=CH2和 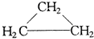 | B. | 乙炔和苯 | C. |  和 和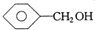 | D. | 葡萄糖与果糖 |
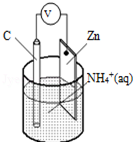 酸性干电池装置示意图如图,电池总反应为:Zn+2NH4+═Zn2++2NH3↑+H2↑,下列说法正确的是( )
酸性干电池装置示意图如图,电池总反应为:Zn+2NH4+═Zn2++2NH3↑+H2↑,下列说法正确的是( )| A. | 碳为电池的负极 | B. | 氨气在碳棒上生成 | ||
| C. | 电流由锌极流向碳极 | D. | H2在Zn片上生成 |
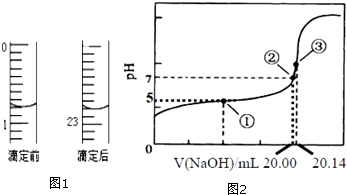 醋酸是日常生活中常见的弱酸.
醋酸是日常生活中常见的弱酸.