题目内容
14.下列属于碱的是( )| A. | Na2SO4 | B. | NaOH | C. | H2SO4 | D. | CO2 |
分析 根据碱的定义及电离的离子的特点进行分析,电离时生成的阴离子都是氢氧根离子的化合物是碱,电离时生成的阳离子都是氢离子的化合物是酸,由金属离子和酸根离子构成的化合物属于盐.
解答 解:A、硫酸钠是由钠离子和硫酸根离子组成的化合物,属于盐,故A不符合;
B、氢氧化钠电离时生成的阴离子都是氢氧根离子,属于碱,故B符合;
C、硫酸为酸不是碱,故C不符合;
D、二氧化碳是由碳和氧两种元素组成的化合物,属于氧化物,故D不符合;
故选B.
点评 本题主要考查物质的分类的知识,解答时要分析物质的阴阳离子构成,然后再根据酸碱盐概念方面进行分析、判断,从而得出正确的结论,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
4.下列反应完毕后有沉淀的是( )
| A. | BaCl2溶液与Na2CO3溶液加足量稀醋酸 | |
| B. | Ba(OH)2溶液与KNO3溶液加足量H2SO4 | |
| C. | AgNO3溶液与Na2CO3溶液加足量稀硝酸 | |
| D. | Ca(OH)2溶液与FeCl3溶液加足量稀硝酸 |
5.下列说法不正确的是( )
| A. | 升高温度可增大单位体积活化分子数百分数,促进有效碰撞,从而提高反应速率 | |
| B. | 增大体系压强可增大单位体积活化分子数,促进有效碰撞,从而提高反应速率 | |
| C. | 放热反应(△H<0)和熵增(△S>0)反应一定能自发反应 | |
| D. | 由能量守恒可知任何放热反应都可设计成原电池 |
2.要除去氯气中的水蒸气,应当使气体通过( )
| A. | 浓硫酸 | B. | 干燥的石灰 | C. | 固体氢氧化钠 | D. | 碱石灰 |
9.用NA表示阿伏伽德罗常数的值,下列说法正确的是( )
| A. | 标准状况下,22.4 L乙烯含有的共用电子对数为5NA | |
| B. | 8.0gCu2S和CuO的混合物中含有的铜原子数为0.1NA | |
| C. | 电解饱和食盐水时,阳极生成22.4L气体时,转移的电子数为2NA | |
| D. | 室温下向1L pH=1的醋酸溶液中加水,所得溶液中H+数目小于0.1NA |
19.下列说法不正确的是( )
| A. | 硅可用于制造电脑芯片 | B. | 浓H2SO4可用做干燥剂 | ||
| C. | 碳酸氢钠可用于食品的发酵 | D. | 少量金属钠保存在酒精中 |
6.短周期元素W、X、Y、Z在元素周期表中的相对位置如表所示,这四种元素的原子最外层电子数之和为21.下列说法不正确的是( )
| W | |||
| X | Y | Z |
| A. | 原子半径大小:X>Y>Z | |
| B. | W、Y两种元素都能与氧元素形成化合物WO2、YO2 | |
| C. | 最高价氧化物对应水化物的酸性:W>Y>Z | |
| D. | W元素的单质能从X的氧化物中置换出X单质 |
11.柠檬烯是一种常用香料,其结构简式如图.有关柠檬烯的分析正确的是( )
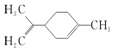

| A. | 它的一氯代物有6种 | |
| B. | 它分子式为:C10H18 | |
| C. | 它的分子中所有的碳原子一定在同一平面上 | |
| D. | 一定条件下,它分别可以发生加成、取代、氧化、加聚等反应 |