题目内容
过氧化钠是一种重要的化合物,常用作呼吸面具中和潜水艇的供氧剂,其化学式为 它与二氧化碳反应的化学方程式为 .
考点:化学方程式的书写,钠的重要化合物
专题:
分析:过氧化钠化学式为,和二氧化碳反应生成碳酸钠和氧气;根据化学方程式书写的步骤:写配注等,写出反应方程式.
解答:
解:过氧化钠和二氧化碳反应生成碳酸钠和氧气,作呼吸面具中和潜水艇的供氧剂,反应的化学方程式为:2Na2O2+2CO2═2Na2CO3+O2;
故答案为:Na2O2;2Na2O2+2CO2═2Na2CO3+O2;
故答案为:Na2O2;2Na2O2+2CO2═2Na2CO3+O2;
点评:本题主要考查学生运用所学化学知识分析和解决实际问题的能力,侧重化学方程式的书写,掌握过氧化钠的性质是解答关键,题目难度不大.

练习册系列答案
相关题目
 在一定条件下,对于反应mA(g)+nB(g)?cC(g)+aD(g),C物质的质量分数[w(C)]与温度,压强的关系如图所示,下列判断正确的是( )
在一定条件下,对于反应mA(g)+nB(g)?cC(g)+aD(g),C物质的质量分数[w(C)]与温度,压强的关系如图所示,下列判断正确的是( )| A、△H>0,m+n>c+d |
| B、△H<0,m+n<c+d |
| C、△H>0,m+n<c+d |
| D、△H<0,m+n>c+d |
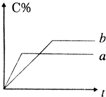 可逆反应A(s)+B(g)?n C (g)△H=Q (n为正整数)在不同条件下反应混合物中C的百分含量和反应过程所需时间的关系曲线如右图所示.下列有关叙述中一定正确的是( )
可逆反应A(s)+B(g)?n C (g)△H=Q (n为正整数)在不同条件下反应混合物中C的百分含量和反应过程所需时间的关系曲线如右图所示.下列有关叙述中一定正确的是( )| A、其他条件相同,a表示使用了催化剂,b没有使用催化剂 |
| B、其他条件相同,若只改变压强,则a比b的压强大且n≥2 |
| C、其他条件相同,若只改变温度,则a比b的温度高且Q>0 |
| D、其他条件相同,a表示减少A的物质的量 |
已知:CH4(g)+H2O(g)=CO(g)+3H2(g)△H=+206kJ?mol-1CH4(g)+CO2(g)=2CO(g)+2H2(g)△H=+247kJ?mol-1
C-H键的键能约为413kJ/mol,O-H键的键能约为463kJ/mol,H-H键的键能约为436kJ/mol,则CO2中C=O键的键能约为( )
C-H键的键能约为413kJ/mol,O-H键的键能约为463kJ/mol,H-H键的键能约为436kJ/mol,则CO2中C=O键的键能约为( )
| A、797.5kJ/mol |
| B、900.5kJ/mol |
| C、962.5kJ/mol |
| D、1595kJ/mol |
利用图示的四种实验装置进行下列实验:海水中提取水、从 KCl溶液中获取KCl晶体、分离CaCO3和水、分离植物油和水.其操作的名称依次是( )
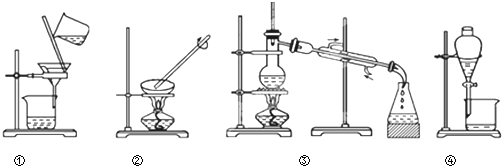

| A、蒸发、蒸馏、过滤、萃取 |
| B、过滤、蒸馏、蒸发、萃取 |
| C、过滤、蒸发、蒸馏、分液 |
| D、蒸馏、蒸发、过滤、分液 |
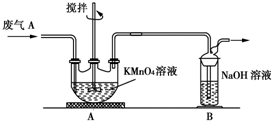 硫酸工业产生的废气A(主要成分:SO2、O2、N2、CO2等)排放到空气中会污染环境.某化学兴趣小组对废气A的组成进行探究,请回答下列问题.
硫酸工业产生的废气A(主要成分:SO2、O2、N2、CO2等)排放到空气中会污染环境.某化学兴趣小组对废气A的组成进行探究,请回答下列问题.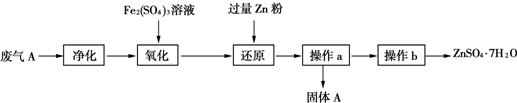
 用实验室准确配制的0.100mol/L的NaOH溶液测定某未知浓度的稀盐酸,其具体实验步骤如下:
用实验室准确配制的0.100mol/L的NaOH溶液测定某未知浓度的稀盐酸,其具体实验步骤如下: