题目内容
20.某一反应体系有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2已知该反应中H2O2只发生如下过程:H2O2→O2①该反应中的氧化剂是H2O2.
②该反应中,发生还原反应的过程是H2CrO4→Cr(OH)3.
③写出该反应的化学方程式,并标出电子转移的方向和数目
 =2Cr(OH)3↓+3O2↑+2H2O.
=2Cr(OH)3↓+3O2↑+2H2O.④如反应转移了0.6mol电子,则产生的气体在标准状况下体积为6.72L.
分析 ①由H2O2只发生如下过程H2O2-→O2可知,利用该过程中O元素的化合价由-1价升高到0来分析;
②氧化剂发生还原反应,利用元素的化合价降低来分析;
③由失去电子的元素指向得到电子的元素,并标出电子转移的总数来用单线桥法标出电子转移的方向和数目;
④由反应可知生成3mol气体转移6mol电子,以此来计算.
解答 解:①由信息H2O2-→O2中可知,O元素的化合价由-1价升高到0,则H2O2为还原剂,故答案为:H2O2;
②氧化剂发生还原反应,含元素化合价降低的物质为氧化剂,则Cr元素的化合价降低,即还原反应的过程为H2CrO4→Cr(OH)3,故答案为:H2CrO4;Cr(OH)3;
③该反应中O元素失电子,Cr元素得到电子,2molH2CrO4反应转移电子为2mol×(6-3)=6mol,则用单线桥法标出电子转移的方向和数目为 =2Cr(OH)3↓+3O2↑+2H2O,
=2Cr(OH)3↓+3O2↑+2H2O,
故答案为: =2Cr(OH)3↓+3O2↑+2H2O;
=2Cr(OH)3↓+3O2↑+2H2O;
④由2H2CrO4+3H2O2═2Cr(OH)3↓+3O2↑+2H2O可知,生成3mol气体转移6mol电子,则转移了0.6mol电子,则产生的气体的物质的量为0.3mol,
其在标准状况下体积为0.3mol×22.4L/mol=6.72L,
故答案为:6.72L.
点评 本题考查氧化还原反应,明确过氧化氢发生的反应及氧化还原反应中既有元素的化合价升高又有元素的化合价降低来分析是解答的关键,然后利用化合价变化来计算电子的转移即可.

练习册系列答案
 新编小学单元自测题系列答案
新编小学单元自测题系列答案
相关题目
11.某有机化合物D的结构为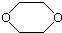 ,是一种常见的有机溶剂,它可以通过下列三步反应制得:
,是一种常见的有机溶剂,它可以通过下列三步反应制得:
烃A$→_{①}^{Br_{2}}$B$→_{②}^{NaOH溶液}$C$→_{③}^{浓硫酸}$D,下列相关说法中正确的是( )
 ,是一种常见的有机溶剂,它可以通过下列三步反应制得:
,是一种常见的有机溶剂,它可以通过下列三步反应制得:烃A$→_{①}^{Br_{2}}$B$→_{②}^{NaOH溶液}$C$→_{③}^{浓硫酸}$D,下列相关说法中正确的是( )
| A. | 烃A为CH3CH3 | B. | 反应②属于消去反应 | ||
| C. | 反应①②③都属于取代反应 | D. | 化合物D属于醚 |
8.在恒温恒容条件下,能使A(g)+2B(g)?C(g)+D (g) 正反应速率增大的措施是( )
| A. | 增大D的浓度 | B. | 减小C的浓度 | C. | 减小B的浓度 | D. | 减小压强 |
15.下列给出的形式能够表示水的电离的是( )
| A. | H2O═H++OH- | B. | 2H2O?H3O++OH- | C. | H2O?2H++O2- | D. | H++OH-═H2O |
5.四种短周期元素在周期表中的相对位置如表所示,其中Z元素原子核外电子总数是其最外层电子数的3倍,下列说法正确的是( )
| X | Y | |
| Z | W |
| A. | 元素W位于第三周期第ⅤA族 | |
| B. | 元素Y的氢化物水溶液呈酸性 | |
| C. | 元素X、Z的各种氯化物分子中,各原子均满足8电子稳定结构 | |
| D. | 元素X与氢元素形成的原子个数比为1:1的化合物有多种 |
12.为了提高氮水中次氯酸的浓度,增强氯水的漂白力,可向氯水中加入的试剂是( )
| A. | CaCO3 | B. | Na2SO3 | C. | H2SO4 | D. | Ca(OH)2 |
 ,B转化为C的离子方程式是Al(OH)3+OH-=AlO2-+2H2O.
,B转化为C的离子方程式是Al(OH)3+OH-=AlO2-+2H2O.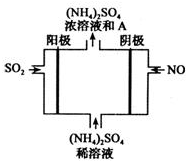 经研究发现,含pM2.5的雾霾主要成分有SO2、NOx、CxHy,及可吸入颗粒等.
经研究发现,含pM2.5的雾霾主要成分有SO2、NOx、CxHy,及可吸入颗粒等.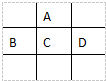 有A、B、C、D、E五种短周期元素,已知相邻的A、B、C、D四种元素原子核外共有56个电子,在周期表中的位置如图所示.E的单质可与酸反应,1mol E单质与足量酸作用,在标准状况下能产生33.6L H2;E的阳离子与A的阴离子核外电子层结构完全相同,回答下列问题:
有A、B、C、D、E五种短周期元素,已知相邻的A、B、C、D四种元素原子核外共有56个电子,在周期表中的位置如图所示.E的单质可与酸反应,1mol E单质与足量酸作用,在标准状况下能产生33.6L H2;E的阳离子与A的阴离子核外电子层结构完全相同,回答下列问题: .
.