题目内容
 A、B、C、X均为中学化学常见物质一定条件下它们有如图转化关系(其他产物已略去).下列说法正确的是( )
A、B、C、X均为中学化学常见物质一定条件下它们有如图转化关系(其他产物已略去).下列说法正确的是( )| A、若X为Fe,则C可能为Fe(NO3 )2 |
| B、若X为KOH溶液,则A可能为Al |
| C、若X为O2,则A可为有机物乙醇,也可为非金属单质硫 |
| D、若A、B、C均为焰色反应呈黄色的化合物,则X一定为CO2 |
考点:无机物的推断
专题:
分析:根据图知,A+X→C,A
B
C,由此看出,A与X反应生成B还是C与X的量有关,
A.若X为Fe,则A可以为HNO3,B为Fe(NO3)3溶液,C可能为Fe(NO3)2溶液;
B.若X为KOH溶液,A为A1时和碱反应只能生成偏氯酸钾;
C.若X为O2,A为有机物乙醇,则B为乙醛,C为乙酸;为非金属单质硫时,则B为二氧化硫,C为三氧化硫,硫和氧气反应不能直接生三氧化硫;
D.若A、B、C均为焰反应呈黄色的化合物,说明含钠元素,转化关系中A可以是NaOH,X可以是二氧化碳或二氧化硫,B为碳酸钠或亚硫酸钠,C为碳酸氢钠或亚硫酸氢钠.
| X |
| X |
A.若X为Fe,则A可以为HNO3,B为Fe(NO3)3溶液,C可能为Fe(NO3)2溶液;
B.若X为KOH溶液,A为A1时和碱反应只能生成偏氯酸钾;
C.若X为O2,A为有机物乙醇,则B为乙醛,C为乙酸;为非金属单质硫时,则B为二氧化硫,C为三氧化硫,硫和氧气反应不能直接生三氧化硫;
D.若A、B、C均为焰反应呈黄色的化合物,说明含钠元素,转化关系中A可以是NaOH,X可以是二氧化碳或二氧化硫,B为碳酸钠或亚硫酸钠,C为碳酸氢钠或亚硫酸氢钠.
解答:
解:A、若X为Fe,则A和铁量不同产物不同,且产物可以和铁反应,证明A为氧化性酸,判断A可以为HNO3,B为Fe(NO3)3溶液,则C可能为Fe(NO3)2溶液,铁与硝酸反应生成硝酸铁,硝酸铁与铁与硝酸来铁,过量的铁与硝酸也可直接生成硝酸亚铁,故A正确;
B、若X为KOH溶液,A为A1时和碱反应只能生成偏氯酸钾,偏铝钾不能和铝反应,不符合转化关系,A可以为Al3+,故B错误;
C、若X为O2,A为有机物乙醇,可以实现A→B→C的转化,但不能一步实现A→C;为非金属单质硫时,可以实现A→B→C的转化,但不能实现A→C的转化,故C错误;
D、若A、B、C均为焰反应呈黄色的化合物,说明含钠元素,转化关系中A可以是NaOH,X可以是二氧化碳或二氧化硫,B为碳酸钠或亚硫酸钠,C为碳酸氢钠或亚硫酸氢钠,故D错误;
故选A.
B、若X为KOH溶液,A为A1时和碱反应只能生成偏氯酸钾,偏铝钾不能和铝反应,不符合转化关系,A可以为Al3+,故B错误;
C、若X为O2,A为有机物乙醇,可以实现A→B→C的转化,但不能一步实现A→C;为非金属单质硫时,可以实现A→B→C的转化,但不能实现A→C的转化,故C错误;
D、若A、B、C均为焰反应呈黄色的化合物,说明含钠元素,转化关系中A可以是NaOH,X可以是二氧化碳或二氧化硫,B为碳酸钠或亚硫酸钠,C为碳酸氢钠或亚硫酸氢钠,故D错误;
故选A.
点评:本题考查了元素化合物性质与转化,注意掌握中学常见连续反应,熟练掌握元素化合物的性质是解题关键.

练习册系列答案
 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案
相关题目
设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A、标准状况下,将22.4 L氯化氢溶于足量水中,溶液中含有的HCl分子数为NA |
| B、常温常压下,16 g 14CH4所含中子数目为8NA |
| C、常温常压下,Na2O2与足量H2O反应,共生成0.2 mol O2,转移电子的数目为0.4 NA |
| D、标准状况下,22.4 L空气含有NA个单质分子 |
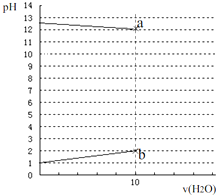 常温下,各1L的 0.1mol?L-1的HX溶液与0.1mol?L-1某一元碱ROH溶液加水稀释,两溶液pH与加水体积变化曲线如图,下列说法正确的是( )
常温下,各1L的 0.1mol?L-1的HX溶液与0.1mol?L-1某一元碱ROH溶液加水稀释,两溶液pH与加水体积变化曲线如图,下列说法正确的是( )| A、HX为一种弱酸,ROH为弱碱 |
| B、a、b两点由水电离出c(H+)均为10-12mol?L-1 |
| C、两溶液等体积混合:c(X-)=c(R+)+c(ROH) |
| D、两溶液等体积混合:c(R+)>c(X-)>c(OH-)>c(H+) |
下列4种醇中,不能被催化氧化的是( )
A、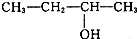 |
B、 |
C、 |
D、 |
下列说法中,错误的是( )
| A、含有离子键的化合物一定是离子化合物 |
| B、含有共价键的化合物一定是共价化合物 |
| C、共价化合物中一定含有极性共价键,肯定不含离子键 |
| D、离子化合物一定含有离子键,可能含有共价键. |
决定乙醇主要化学性质的原子或原子团是( )
| A、羟基 | B、乙基 |
| C、氢氧根离子 | D、氢离子 |
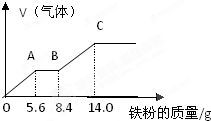 某稀硫酸和稀硝酸的混合溶液100mL,向其中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示(已知硝酸的还原产物只有NO气体)
某稀硫酸和稀硝酸的混合溶液100mL,向其中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示(已知硝酸的还原产物只有NO气体)