题目内容
质量分数为m%的NaOH溶液,其物质的量浓度为a mol/L,加热蒸发水使其质量分数变为2m%,此时,该溶液中NaOH的物质的量浓度为b mol/L,则a与b的关系正确的是( )
| A、b=2a | B、a=2b |
| C、b>2a | D、b<2a |
考点:物质的量浓度的相关计算
专题:
分析:设质量分数为m%的NaOH溶液的密度为d g/mL,质量分数为2m%的NaOH溶液的密度为D g/mL,根据c=
表示出各自物质的量浓度,氢氧化钠溶液的浓度越大,密度越大,则D>d,结合密度进行判断.
| 1000ρω |
| M |
解答:
解:设质量分数为m%的NaOH溶液的密度为d g/mL,质量分数为2m%的NaOH溶液的密度为D g/mL,
根据c=
可知,a=
,b=
,
氢氧化钠溶液的浓度越大,密度越大,则D>d,故b>2a,
故选C.
根据c=
| 1000ρω |
| M |
| 1000×d×m% |
| 40 |
| 1000×D×2m% |
| 40 |
氢氧化钠溶液的浓度越大,密度越大,则D>d,故b>2a,
故选C.
点评:本题考查溶液浓度有关计算,涉及物质的量浓度、质量分数计算,注意理解掌握物质的量浓度与质量分数之间的关系.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
核磁共振氢谱是指有机物分子中的氢原子核所处的化学环境(即其附近的基团)不同,表现出的核磁性就不同,代表核磁性特征的峰在核磁共振氢谱图中坐标的位置(化学位移,符号为δ)也就不同.现有一物质的核磁共振氢谱如下图所示,则它可能是( )
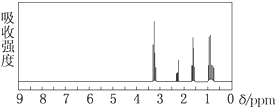

| A、CH3CH2CH3 |
| B、CH3CH2CH2OH |
| C、(CH3)2CHCH3 |
| D、CH3CH2CHO |
为比较盐酸与醋酸的酸性强弱,下列方案不可行的是(均在常温下测定)( )
| A、比较等体积、等pH值的两种溶液的导电性 |
| B、比较等物质的量浓度的氯化钠与醋酸钠溶液的pH值 |
| C、比较等体积、等pH值的两种溶液与过量锌粉反应产生氢气的量 |
| D、比较等体积、等物质的量浓度的两种溶液稀释相同倍数后的pH变化 |
下列两分子的关系是( )
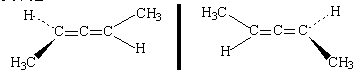
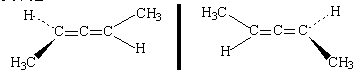
| A、互为同素形体 |
| B、同一物质 |
| C、手性异构体 |
| D、互为同系物 |
下列有关碳酸钠在化学实验中的作用叙述错误的是( )
| A、用碳酸钠溶液制备少量烧碱 |
| B、用热的碳酸钠溶液洗涤试管内壁的油污 |
| C、用饱和碳酸钠溶液除去CO2中混有的HCl气体 |
| D、用饱和碳酸钠溶液除去乙酸乙酯中混有的乙醇和乙酸 |
下列有关溶液和胶体的叙述正确的是( )
| A、Fe(OH)3胶体和FeCl3溶液区别的本质特征为是否具有丁达尔效应 |
| B、FeCl3溶液呈电中性,Fe(OH)3胶体带有电荷 |
| C、纳米材料的微粒直径一般从几纳米到几十纳米,因此纳米材料是胶体 |
| D、FeCl3溶液能使血液凝聚沉降 |
 在200mL含Mg2+、Al3+、NH4+、H+、Cl-等离子的溶液中,逐滴加入5mol?L-1的NaOH溶液,所加NaOH溶液的体积与产生沉淀的物质的量关系如图所示.下列叙述错误的是( )
在200mL含Mg2+、Al3+、NH4+、H+、Cl-等离子的溶液中,逐滴加入5mol?L-1的NaOH溶液,所加NaOH溶液的体积与产生沉淀的物质的量关系如图所示.下列叙述错误的是( )| A、x与y的差值为0.01mol |
| B、原溶液中c(Cl-)=0.85mol?L-1 |
| C、原溶液的c(H+)=0.1mol?L-1 |
| D、原溶液中n(Mg2+):n(Al3+)=5:1 |