��Ŀ����
��ѧ����Ϊ��������һ�ָ�Ч������Ⱦ��������Դ����20����������������Ϊδ���Ķ���ȼ������Դ���о������Ѹ�ٷ�չ��
��1��Ϊ����Ч��չ��������Դ�����ȱ����Ƶ����۵����������пɹ������ֽϾ�������Դ�ɳ������õ��������ķ����� ����ѡ����ĸ��
A�����ˮ B��п��ϡ���ᷴӦ
C����⺣ˮ D���ֽ���Ȼ��
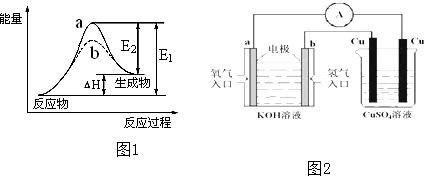
��2����ˮ�ֽ��������������仯��ͼ1��ʾ����ʾʹ�ô��������� ���÷�ӦΪ �����Ȼ������ȣ���Ӧ
��3��1g��������ȫȼ������Һ̬ˮ�ͷų�142.9kJ��������д������ȫȼ�յ��Ȼ�ѧ����ʽ�� ��
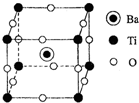
��4������ȼ�ϵ������ת���ʸߣ����й����ķ�չǰ������������ȼ�ϵ�ؽ���ͼ2��ʾʵ�飺ͼ2װ���У�ijһͭ�缫���������� 6.4g����a�������ĵ�O2�ڱ�״���µ����Ϊ L��

��1��Ϊ����Ч��չ��������Դ�����ȱ����Ƶ����۵����������пɹ������ֽϾ�������Դ�ɳ������õ��������ķ�����
A�����ˮ B��п��ϡ���ᷴӦ
C����⺣ˮ D���ֽ���Ȼ��
��2����ˮ�ֽ��������������仯��ͼ1��ʾ����ʾʹ�ô���������
��3��1g��������ȫȼ������Һ̬ˮ�ͷų�142.9kJ��������д������ȫȼ�յ��Ȼ�ѧ����ʽ��
��4������ȼ�ϵ������ת���ʸߣ����й����ķ�չǰ������������ȼ�ϵ�ؽ���ͼ2��ʾʵ�飺ͼ2װ���У�ijһͭ�缫���������� 6.4g����a�������ĵ�O2�ڱ�״���µ����Ϊ
���㣺ԭ��غ͵��صĹ���ԭ��,��Ӧ�Ⱥ��ʱ�,�Ȼ�ѧ����ʽ
ר�⣺��ѧ��Ӧ�е������仯
��������1�������Ͼ�������Դ�ɳ������õ�������������������ԴԽ��Խ�ã�
��2�������ܽ��ͷ�Ӧ��ܣ�����Ӧ������������������������ʱ���÷�Ӧ�Ƿ��ȷ�Ӧ������Ӧ��������С��������������ʱ���÷�Ӧ�����ȷ�Ӧ��
��3��1g���������ʵ���Ϊ0.5mol��1g������ȫȼ������Һ̬ˮ�ͷų�142.9kJ����������2mol������ȫȼ������Һ̬ˮ�ų�����=
��2mol=571.6 kJ���ݴ���д���Ȼ�ѧ��Ӧ����ʽ��
��4��ͭ�缫��������6.4g����ת�Ƶ��ӵ����ʵ���=
��2=0.2mol������ת�Ƶ����غ�����������������
��2�������ܽ��ͷ�Ӧ��ܣ�����Ӧ������������������������ʱ���÷�Ӧ�Ƿ��ȷ�Ӧ������Ӧ��������С��������������ʱ���÷�Ӧ�����ȷ�Ӧ��
��3��1g���������ʵ���Ϊ0.5mol��1g������ȫȼ������Һ̬ˮ�ͷų�142.9kJ����������2mol������ȫȼ������Һ̬ˮ�ų�����=
| 142.9kJ |
| 0.5mol |
��4��ͭ�缫��������6.4g����ת�Ƶ��ӵ����ʵ���=
| 6.4g |
| 64g/mol |
���
�⣺��1�������Ͼ�������Դ�ɳ������õ�������������������ԴԽ��Խ�ã�
A�����ˮ�˷���Դ�����Ը÷������ã��ʲ�ѡ��
B��п��ϡ����۸�ϸߣ������ã����Ը÷������ã��ʲ�ѡ��
C����⺣ˮ��Դ���ĵͣ����ã��÷����ã���ѡ��
D���ֽ���Ȼ���˷���Դ�����Ը÷������ã��ʲ�ѡ��
��ѡC��
��2�������ܽ��ͷ�Ӧ��ܣ�����b����ʹ�ô��������ݷ�Ӧ�����������������Դ�С֪���÷�Ӧ�����ȷ�Ӧ���ʴ�Ϊ��b�����ȣ�
��3��1g���������ʵ���Ϊ0.5mol��1g������ȫȼ������Һ̬ˮ�ͷų�142.9kJ����������2mol������ȫȼ������Һ̬ˮ�ų�����=
��2mol=571.6 kJ�����Ȼ�ѧ��Ӧ����ʽΪ��2H2��g��+O2��g��=2H2O��l����H=-571.6 kJ?mol-1 �����������𰸾��ɣ����ʴ�Ϊ��2H2��g��+O2��g��=2H2O��l����H=-571.6 kJ?mol-1 �����������𰸾��ɣ���
��4��ͭ�缫��������6.4g����ת�Ƶ��ӵ����ʵ���=
��2=0.2mol��ͨ�������ĵ缫��ӦʽΪO2+4e-+2H2O=4OH-������ת�Ƶ�����ȵã�
��ͨ���������ΪV��
O2+4e-+2H2O=4OH-
22.4L 4mol
V 0.2mol
22.4L��4mol=V��0.2mol
V=
=1.12L��
�ʴ�Ϊ��1.12��
A�����ˮ�˷���Դ�����Ը÷������ã��ʲ�ѡ��
B��п��ϡ����۸�ϸߣ������ã����Ը÷������ã��ʲ�ѡ��
C����⺣ˮ��Դ���ĵͣ����ã��÷����ã���ѡ��
D���ֽ���Ȼ���˷���Դ�����Ը÷������ã��ʲ�ѡ��
��ѡC��
��2�������ܽ��ͷ�Ӧ��ܣ�����b����ʹ�ô��������ݷ�Ӧ�����������������Դ�С֪���÷�Ӧ�����ȷ�Ӧ���ʴ�Ϊ��b�����ȣ�
��3��1g���������ʵ���Ϊ0.5mol��1g������ȫȼ������Һ̬ˮ�ͷų�142.9kJ����������2mol������ȫȼ������Һ̬ˮ�ų�����=
| 142.9kJ |
| 0.5mol |
��4��ͭ�缫��������6.4g����ת�Ƶ��ӵ����ʵ���=
| 6.4g |
| 64g/mol |
��ͨ���������ΪV��
O2+4e-+2H2O=4OH-
22.4L 4mol
V 0.2mol
22.4L��4mol=V��0.2mol
V=
| 22.4L��0.2mol |
| 4mol |
�ʴ�Ϊ��1.12��
���������⿼����ۺϣ��漰ԭ��غ͵���ԭ����ȼ���Ȼ�ѧ��Ӧ����ʽ����д�����������õ�֪ʶ�㣬����ת�Ƶ�����Ƚ��е��ء�ԭ��ط�Ӧ�ļ��㣬֪�������ܸı��ܣ������ı䷴Ӧ�ȣ���Ŀ�ѶȲ���

��ϰ��ϵ�д�
 �߽�������ϵ�д�
�߽�������ϵ�д�
�����Ŀ
����ʵ�����ô��Լ����ǣ�������
| A����ϡ����ϴȥ�������Թܱ��ϵ�ͭ |
| B����Ũ�������հ����е�ˮ���� |
| C����ϡ������ϴ����ɫ��Ӧ�IJ�˿ |
| D����Ũ�������������е�ˮ���� |
 �Ѽ��仯���ﱻ�㷺Ӧ���ڷɻ�����������ǡ���ͧ��ҽ���Լ�ʯ�ͻ����������������ý��ʯ����Ҫ�ɷ�ΪTiO2���Ʊ������Ѻ����ᱵ�����̣�
�Ѽ��仯���ﱻ�㷺Ӧ���ڷɻ�����������ǡ���ͧ��ҽ���Լ�ʯ�ͻ����������������ý��ʯ����Ҫ�ɷ�ΪTiO2���Ʊ������Ѻ����ᱵ�����̣�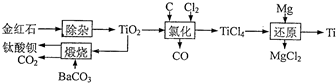
 ��һ�ܱ���ϵ�з������з�ӦA��g��+3B��g��?2C��g����H��0����ͼ��ijһʱ����з�Ӧ�����뷴Ӧ���̵����߹�ϵ������������⣺
��һ�ܱ���ϵ�з������з�ӦA��g��+3B��g��?2C��g����H��0����ͼ��ijһʱ����з�Ӧ�����뷴Ӧ���̵����߹�ϵ������������⣺