题目内容
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A、1.0 mol?L-1KNO3溶液:H+、Fe 2+、SCN -、SO42- | ||
| B、pH=0的溶液:Al3+、Cu(NH3)42+、F -、SO42- | ||
| C、c(ClO-)=1.0mol?L-1的溶液:Na+、SO32-、S2-、SO42- | ||
D、
|
考点:离子共存问题
专题:离子反应专题
分析:A.硝酸盐在酸性条件下具有强氧化性;
B.pH=0的溶液,显酸性;
C.离子之间发生氧化还原反应;
D.
=10 -10的溶液,溶液显碱性.
B.pH=0的溶液,显酸性;
C.离子之间发生氧化还原反应;
D.
| c(H+) |
| c(OH-) |
解答:
解:A.H+、NO3-会将Fe 2+氧化成Fe3+,与SCN -不共存,故A错误;
B.pH=0说明溶液呈酸性,不能与F-共存生成弱电解质,故B错误;
C.ClO-具有氧化性,与SO32-、S2-不共存,故C错误;
D.
=10 -10的溶液,溶液显碱性,四种离子之间不反应,可大量共存,故D正确;
故选D.
B.pH=0说明溶液呈酸性,不能与F-共存生成弱电解质,故B错误;
C.ClO-具有氧化性,与SO32-、S2-不共存,故C错误;
D.
| c(H+) |
| c(OH-) |
故选D.
点评:本题考查离子的共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重复分解反应、氧化还原反应的离子共存考查,注意根据题干判断溶液具有的性质如酸性、碱性、氧化性等,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列物质在空气中不能稳定存在的是( )
| A、Fe(OH)2 |
| B、Fe(OH)3 |
| C、K3Fe(CN)6 |
| D、Cu(NH3)4SO4 |
 北京奥运会期间对大量盆栽鲜花施用了S-诱抗素制剂,以保持鲜花盛开.S-诱抗素的分子结构如图,下列说法正确的( )
北京奥运会期间对大量盆栽鲜花施用了S-诱抗素制剂,以保持鲜花盛开.S-诱抗素的分子结构如图,下列说法正确的( )| A、此有机物含有如下的官能团:含有碳碳双键、羟基、羰基、羧基 |
| B、1mol该有机物与NaOH 溶液反应,耗2mol.与氢气反应耗氢气5mol |
| C、该有机分子中没有一个有手性碳 |
| D、该有机物不存在顺反异构 |
如图所示是298K时,N2与H2反应过程中能量变化的曲线图,下列叙述正确的是( )
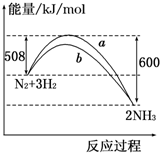

| A、该反应的热化学方程式为:N2+3H2?2NH3△H=-92 kJ/mol |
| B、a曲线是加入催化剂时的能量变化曲线 |
| C、加入催化剂,该化学反应的反应热改变 |
| D、在温度、体积一定的条件下,若通入2 mol N2和6 mol H2反应后放出的热量为Q kJ,则184>Q |
萃取碘水中碘时,选用CCl4作为萃取剂理由不正确的是( )
| A、CCl4与原溶剂水互不溶解 |
| B、CCl4与水和碘都不发生化学反应 |
| C、CCl4是有机溶剂,且密度比水大 |
| D、碘在CCl4中的溶解度比在水中的大得多 |
菲的结构简式可表示为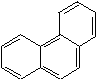 ,若菲分子中有1个H原子被Cl原子取代,则所得一氯取代产物有( )
,若菲分子中有1个H原子被Cl原子取代,则所得一氯取代产物有( )
 ,若菲分子中有1个H原子被Cl原子取代,则所得一氯取代产物有( )
,若菲分子中有1个H原子被Cl原子取代,则所得一氯取代产物有( )| A、4种 | B、5种 | C、6种 | D、7种 |
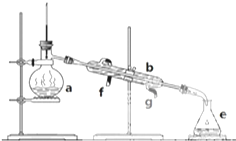 掌握仪器名称、组装及使用方法是中学化学实验的基础,图为实验装置.
掌握仪器名称、组装及使用方法是中学化学实验的基础,图为实验装置.