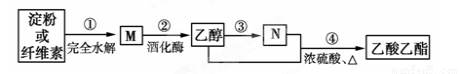
题目内容
(14分)有A、B、C、D四种物质,B的焰色反应为黄色。C是酸式盐,C加入硝酸酸化的Ba(NO3)2溶液中有白色沉淀生成。D和G相遇有大量白烟生成,D通入硝酸酸化的AgNO3溶液有白色沉淀生成。对A、B、C、D四种物质的水溶液进行下列实验,过程和现象如下图所示(图中部分产物未列出),请回答下列问题:

(1)B的电子式为____________________。
(2)H生成I的化学方程式为 。
(3)G在同主族同类物质中稳定性最强____,也是沸点最高的 。(判断正误填“是”或“否”)
(4)A溶液中加入D,A溶液的颜色由浅绿色变黄,则A的化学式为__________ 。
(5)写出C与过量B反应(加热)的离子方程式 。
(6)C与D溶液恰好反应,假设生成气体全部逸出,所得溶液中离子浓度从大到小的顺序 。
(7)25℃时pH=9的B溶液和pH=9的G溶液中,水的电离程度B___________G(填>,<或=)。
(1)略(2)2SO2+O2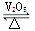 2SO3 (3) 是;否 (4)Fe(NO3)2
2SO3 (3) 是;否 (4)Fe(NO3)2
(5) NH4++HSO3-+2OH-  NH3 ↑+SO32-+2H2O
NH3 ↑+SO32-+2H2O
(6) [Cl-]>[NH4+]>[H+]>[OH- ] (7) =
【解析】
试题分析:能使紫色石蕊溶液变蓝的无色气体G为NH3 ,发生反应能生成氨气的是铵盐与强碱反应,C加入硝酸酸化的Ba(NO3)2溶液中有白色沉淀生成且C是酸式盐,则C为亚硫酸氢铵,B的焰色反应为黄色,则B为NaOH,(1)D和G相遇有大量白烟生成,D为盐酸或硝酸,D通入硝酸酸化的AgNO3溶液有白色沉淀生成,则D为盐酸,白色沉淀E在空气中变成红褐色沉淀F(红褐色沉淀为Fe(OH)3),则A为硝酸亚铁。(3)同主族元素气态氢化物的稳定性逐渐减弱,所以G在同主族同类物质中稳定性最强,同主族元素气态氢化物的沸点逐渐升高,NH3因存在氢键略有增加,所以氨气的沸点最高错误(4)A溶液中加入D(盐酸),A溶液的颜色由浅绿色(Fe2+的颜色)变黄(Fe3+的颜色),说明两种溶液混合后有氧化性,所以A为Fe(NO3)2 (5) 亚硫酸氢铵与过量NaOH溶液反应(以少定多),方程式为:NH4++HSO3-+2OH-  NH3 ↑+SO32-+2H2O(6)C与D溶液恰好反应,所得溶液为NH4Cl溶液,强酸弱碱盐,所以离子浓度排序为:[Cl-]>[NH4+]>[H+]>[OH- ] (7) pH=9的NaOH溶液与PH=9的氨水,它们为碱,对水的电离起到同等程度的抑制作用,所以水的电离程度B=G
NH3 ↑+SO32-+2H2O(6)C与D溶液恰好反应,所得溶液为NH4Cl溶液,强酸弱碱盐,所以离子浓度排序为:[Cl-]>[NH4+]>[H+]>[OH- ] (7) pH=9的NaOH溶液与PH=9的氨水,它们为碱,对水的电离起到同等程度的抑制作用,所以水的电离程度B=G
考点:考察元素与化合物,物质的推断,盐的水解,离子方程式的书写等知识。

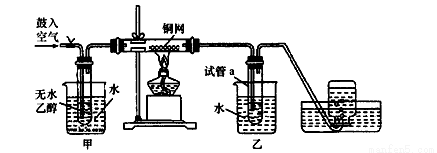
Ⅰ(本题9分)乙酸乙酯是重要的工业原料和溶剂,通常混有少许乙醇和乙酸。某学习小组利用图1装置制取乙酸乙酯粗产品,再分析乙酸乙酯的含量。

| 乙酸乙酯 | 乙醇 | 乙酸 |
沸点 | 77.1℃ | 78.5℃ | 117.9℃ |
操作步骤如下:
(I)准确称量20.0g乙酸乙酯粗品于锥形瓶中,用0.50mol/LNaOH滴定(酚酞做指示剂)。终点时消耗NaOH溶液的体积为40.0mL
(II)另取20.0g乙酸乙酯粗产品于250mL锥形瓶中,加入100mL 2.1mol/LNaOH溶液混合均匀后,装上冷凝箱,在水浴上加热回流约1小时,装置如图2所示。待冷却后,用0.50mol/LHCl滴定过量的NaOH。终点时消耗盐酸的体积为20.0mL。
回答下列问题:
(1)实验(II)中冷水从冷水凝管的 (填a或b)管口通入。
(2)利用实验(I)、(II)测量的数据计算粗产物中乙酸乙酯的质量分数为 。
(3)实验结束后,同学们对粗产品中乙酸乙酯的含量不高进行讨论。
①有人认为是实验(II)带来的误差。建议将图2中的锥形瓶改为三颈瓶,装置如图3,在三颈瓶的c、d口装配相关的仪器并进行恰当的操作,可以提高测定的精确度。你认为在三颈瓶的c、d口装配相关的仪器或操作是: (填字母);
A.装上温度计,严格控制反应温度
B.实验中经常打开瓶口,用玻璃进行搅拌
C.在反应后期,用事先安装的分液漏斗添加一定量的NaOH溶液
②还有同学认为改进乙酸乙酯的制取装置(图1)才能提高产率。拟出你的一条改进建议
Ⅱ(本题6分)如图是配制50 mL酸性KMnO4标准溶液的过程示意图。

(1)请你观察图示判断其中不正确的操作有________(填序号)。
(2)其中确定50 mL溶液体积的容器是____________________________________(填名称)。
(3)如果按照图示的操作所配制的溶液进行实验,在其他操作均正确的情况下,所测得的实验结果将________(填“偏大”或“偏小”)。