题目内容
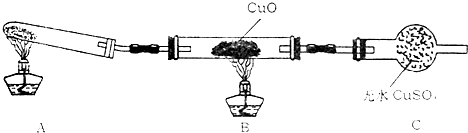
某同学采用萃取-分液的方法从碘水中提取碘,主要操作步骤如图:

(1)该同学所采用的萃取剂可能是 (填“A”、“B”、或“C”).
A.酒精 B.汽油 C.四氯化碳
(2)甲、乙、丙3步实验操作中,不正确的是 (填“甲”、“乙”、或“丙”).

(1)该同学所采用的萃取剂可能是
A.酒精 B.汽油 C.四氯化碳
(2)甲、乙、丙3步实验操作中,不正确的是
考点:分液和萃取
专题:
分析:(1)从碘水中提取碘,萃取剂不能与水混溶,有机层在下层;
(2)分离时先分离下层液体.
(2)分离时先分离下层液体.
解答:
解:(1)从碘水中提取碘,萃取剂不能与水混溶,而酒精与水混溶,不能作萃取剂;有机层在下层,汽油密度比水小,只有四氯化碳符合,故答案为:C;
(2)振荡、静置分层操持合理,而分离时先分离下层液体后倒出上层液体,则丙图不合理,故答案为:丙.
(2)振荡、静置分层操持合理,而分离时先分离下层液体后倒出上层液体,则丙图不合理,故答案为:丙.
点评:本题考查物质分离、提纯方法的选择,为高频考点,侧重分液和萃取、除杂及尾气处理的考查,明确萃取剂的选择及氯气的实验室制法为解答的关键,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列说法正确的是( )
| A、CCl4曾用作灭火剂,但因与水在高温下反应会产生有毒物质,现已被禁用 |
| B、蔗糖、油脂及它们的水解产物均为非电解质 |
| C、棉花、羊毛、腈纶和涤纶都属于合成纤维 |
| D、将纳米材料分散到液体分散剂中,该分散系可发生丁达尔现象,可推测纳米材料的直径为1~100nm之间 |
20世纪90年代,国际上提出了“预防污染”这一新概念.绿色化学是“预防污染”的基本手段.下列各项中属于绿色化学的是( )
| A、杜绝污染源 |
| B、减少有害物质 |
| C、治理污染点 |
| D、处理废弃物 |
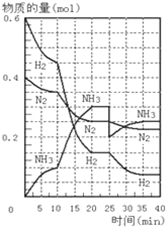 500℃、20MPa时,将H2和N2置于一容积为2L的密闭容器中发生反应:3H2+N2?2NH3△H<0.反应过程中H2、N2和NH3物质的量变化如图所示,据图判断下列叙述不正确的是( )
500℃、20MPa时,将H2和N2置于一容积为2L的密闭容器中发生反应:3H2+N2?2NH3△H<0.反应过程中H2、N2和NH3物质的量变化如图所示,据图判断下列叙述不正确的是( )| A、反应开始到第一次平衡时,N2的平均反应速率为0.0625mol?(L?min)-1,H2的转化率为75% |
| B、反应达到第一次平衡时,反应的平衡常数表达式可写作:K=c2(NH3)/[c3(H2)?c(N2)]=(0.15 mol?L-1)2/[(0.075 mol?L-1)3?(0.125 mol?L-1)] |
| C、从曲线变化可以看出,反应进行到10min至20min时可能采取的措施是使用了催化剂 |
| D、从曲线变化可以看出,反应进行至25min时,采取的措施是分离出0.1mol的氨气,平衡正向移动 |
元素及其化合物丰富了物质世界,下列说法正确的是( )
| A、铜在冷的浓硫酸中会钝化,所以把铜放入冷的浓硫酸中无明显现象 |
| B、NaOH溶液和AlCl3溶液相互滴加的现象不同 |
| C、金属比非金属易失电子,所以金属可以置换非金属,而非金属不能置换金属 |
| D、Al与热水反应困难,故活泼性不及Al的金属在任何条件下均不能与H2O发生反应 |
一些装有化学物质的瓶子上贴有危险警告标签,下面是一些危险警告标签,其中贴法有错误的是( )
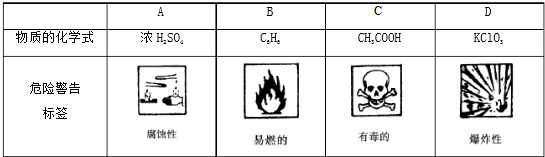

| A、A | B、B | C、C | D、D |
下列离子方程式正确的是( )
| A、NaClO溶液与FeCl2溶液混合:Fe2++2ClO-+2H2O═Fe(OH)2↓+2HClO |
| B、NH4HSO3溶液与足量NaOH溶液共热:NH4++H++2OH-═NH3↑+2H2O |
| C、向1L 1mol/L碘化亚铁溶液中通入标准状况下22.4L氯气:2Fe2+-+Cl2═2Fe3+2Cl- |
| D、澄清石灰水与少量的小苏打溶液混合:Ca2++OH-+HCO3-═CaCO3↓+H2O |