��Ŀ����
18��CO2��һ����Ҫ���������壬�о�CO2�����öԴٽ���̼���Ĺ���������Ҫ�����壮��1�����ʯ��ʯīȼ�շ�Ӧ�е������仯��ͼ1��ʾ��
����ͨ��״���£����ʯ��ʯī�У�ʯī������ʯ����ʯī�������ȶ���ʯī��ȼ����Ϊ393.5kJ•mol-1��
��ʯī��CO2��Ӧ����CO���Ȼ�ѧ����ʽ��C��s��+CO2��g��=2CO��g����H=+172.5 kJ•mol-1
��2�����õ绯ѧ���ɽ�CO2ת��Ϊ���飮��д������������ˮ��Һ�������ʱ����ת���ĵ缫��Ӧ����ʽCO2+8e-+6H2O=CH4+8OH-
��3��CO2Ϊԭ�ϻ��ɺϳɶ������ʣ���ҵ�ϳ���CO2��g����H2��g��Ϊԭ�Ϻϳ��Ҵ���
����֪��H2O��l��=H2O��g����H=+44kJ•mol-1
CO��g��+H2O��g��?CO2��g��+H2��g����H=-41.2kJ•mol-1
2CO��g��+4H2��g��?CH3CH2OH��g��+H2O��g����H=-256.1kJ•mol-1��
��2CO2��g��+6H2��g��?CH3CH2OH��g��+3H2O��l����H=-305.7kJ•mol-1
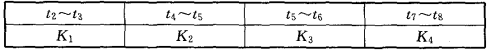
��ͼ2��ʾ��һ������ȼ�ϵ�ؾƾ�����ǣ������Զ����������������ƵĹ��ܣ��dz��ʺϽ����ֳ��ƾ���⣮�õ�ظ����ĵ缫��ӦΪCH3CH2OH-4e-+H2O=4H++CH3COOH
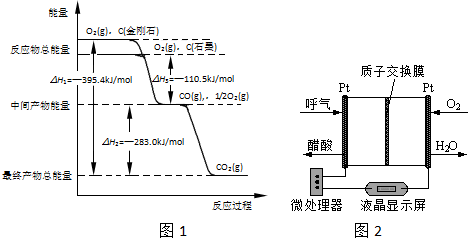
���� ��1����ͼ�����˵��ʯī�������ڽ��ʯ������ȼ���ȸ�����1mol��ȼ����ȫȼ�������ȶ�������ų����������㣻
������ʯīȼ������һ����̼�Ȼ�ѧ����ʽ��һ����̼ȼ�����ɶ�����̼�Ȼ�ѧ����ʽ��ϸ�˹���ɼ���õ������û�ѧ����ʽ��
��2������ԭ���ԭ����CO2������������ԭ��Ӧת��Ϊ���飬ע��������ҺΪ���ԣ�
��3���������Ȼ�ѧ����ʽ��˹���ɼ���õ���
������ȼ�ϵ�ؾƾ�����ǣ�����װ��ͼ��֪�ƾ��ڸ�����������������������Ӧ���ɴ��ᣮ
��� �⣺��1����ͼ�����˵��ʯī�������ڽ��ʯ����������Խ��Խ�ȶ�������ʯī�ȶ�������ȼ���ȸ�����1mol��ȼ����ȫȼ�������ȶ�������ų���������ͼ���������õ�һ����̼ȼ����=E2+E3=110.5LKJ/mol+283.0KJ/mol=393.5KJ/mol��
�ʴ�Ϊ��ʯī��393.5��
��ʯīȼ������һ����̼�Ȼ�ѧ����ʽ��a��C��s��ʯī��+$\frac{1}{2}$O2��g��=CO��g����H=-110.5KJ/mol��
һ����̼ȼ�����ɶ�����̼�Ȼ�ѧ����ʽ��b��CO��g��+$\frac{1}{2}$O2��g��=CO2��g����H=-283.0KJ/mol��
��ϸ�˹���ɼ��㣬a-b�õ������û�ѧ����ʽ��C��s��ʯī��+CO2��g��=2CO��g����H=+172.5kJ•mol-1 ��
�ʴ�Ϊ��C��s��+CO2��g��=2CO��g����H=+172.5 kJ•mol-1��
��2��CO2������������ԭ��Ӧת��Ϊ���飬�缫��ӦΪ��CO2+8e-+6H2O=CH4+8OH-���ʴ�Ϊ��CO2+8e-+6H2O=CH4+8OH-��
��3����a��H2O��l��=H2O��g����H=+44kJ•mol-1
b��CO��g��+H2O��g��?CO2��g��+H2��g����H=-41.2kJ•mol-1
c��2CO��g��+4H2 ��g��?CH3CH2OH��g��+H2O��g����H=-256.1kJ•mol-1
���ݸ�˹����c-b��2-3a�õ���2CO2��g��+6H2��g��?CH3CH2OH��g��+3H2O��l����H=-305.7kJ•mol-1 ��
�ʴ�Ϊ��-305.7kJ•mol-1 ��
�ھƾ�����ǣ�����װ��ͼ��֪�ƾ��ڸ�����������������������Ӧ���ɴ��ᣬCH3CH2OH-4e-+H2O=4H++CH3COOH��
�ʴ�Ϊ��CH3CH2OH-4e-+H2O=4H++CH3COOH��
���� ���⿼���˻�ѧ��Ӧ�����仯��ԭ��ء�����ԭ������Ӧ�ã��Ȼ�ѧ����ʽ����ⷴӦ����ʽ����дʽ����ؼ�����Ŀ�Ѷ��еȣ�

| A�� | �ü��ȡ����صķ�������Na2CO3�����NaHCO3���� | |
| B�� | ����ɫ��Ӧ����NaCl�����NaOH���� | |
| C�� | ij��Һ�еμ������ܲ�����ɫ���壬��������ʹ����ʯ��ˮ����ǣ���ԭ��Һ��һ����CO32- | |
| D�� | ��ij��Һ�м���BaCl2��Һ���ְ�ɫ�������ټ���HCl��Һ����ɫ�������ܽ⣬�����Һ�п϶���SO42- |
| A�� | ̼��ĵ��뷽��ʽ��H2CO3�T2H++CO32- | |
| B�� | NaHSO4����Һ���ĵ��룺NaHSO4�TNa++H++SO42- | |
| C�� | ��������ˮ������ӷ���ʽ��SO32-+2H2O?H2SO3+2OH- | |
| D�� | HCO3-��ˮ�ⷽ��ʽΪ��HCO3-+H2O?CO32-+H3O+ |
| A�� | �������ʵ�����KHC2O4��H2C2O4����ˮ�����Һ��2c��K+���Tc��HC2O4-��+c��H2C2O4�� | |
| B�� | 0.1 mol•L-1NH4Cl��Һ��0.1 mol•L-1��ˮ�������ϣ�pH��7����c��NH3•H2O����c��NH${\;}_{4}^{+}$����c��Cl-����c��OH-�� | |
| C�� | 0.1mol/L��CH3COOH��Һ��ˮϡ�ͣ�$\frac{c��{H}^{+}��}{c��C{H}_{3}CO{O}^{-}��}$�ı�ֵ������ | |
| D�� | 0.1mol/LCH3COONa��Һ��0.15mol/LHCl�������ϣ�c��Cl-����c��H+����c��Na+����c��CH3COO-����c��OH-�� |
| A�� | $\frac{18}{{N}_{A}}$ | B�� | $\frac{18}{{N}_{A}}$g•mol-1 | C�� | 18NA g | D�� | $\frac{18}{{N}_{A}}$g |
| A�� | 22.4g | B�� | 11.2g | C�� | 20.4g | D�� | 5.6g |
| A�� | ʵ���ұ����ʯʱӦע���ܷ⣬�������������ﴦ | |
| B�� | ������Ӧ����1molC2H2�����ڳ��³�ѹ�����Ϊ2.24L | |
| C�� | ��ʯ��ˮ��Ӧ����������ԭ��Ӧ | |
| D�� | ����C2H2������� |
 ����
����
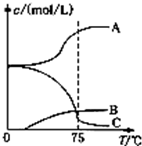 �����ƣ�NaClO3�������ι�ҵ����Ҫ��Ʒ֮һ��
�����ƣ�NaClO3�������ι�ҵ����Ҫ��Ʒ֮һ��