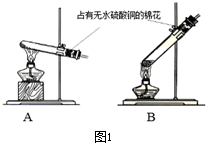
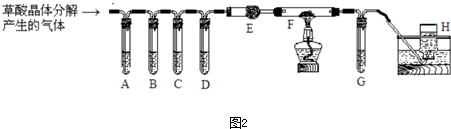
��Ŀ����
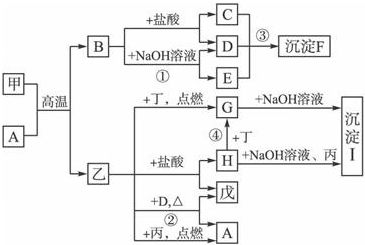
��ҩ��ҵ�г��õ����������Σ�������ɿɷֱ��ʾΪFeXY3��FeX2Y4���ֱ�����������ȼס��ң�������FeY��XY2��������FeY��XY2��XY��XY2����������ЧӦ����Ҫ���壮��ʪ�ļ��ڿ�����ˮ�⣬���ɰ�ɫ����D��XY2��D�ڿ�����Ѹ�ٱ�ɻ���ɫ�����ձ�ɺ��ɫ��
��1����ɫ����D�Ļ�ѧʽΪ ���Ļ�ѧʽΪ ��
��2���Ҽ��ȷֽ�Ļ�ѧ����ʽΪ
��3����������ϡ�����У��������������壬�÷�Ӧ�����ӷ���ʽΪ
��4�������ʵ�鷽����֤��ʪ�ļ�¶���ڿ������Ƿ���ʣ� ��
��1����ɫ����D�Ļ�ѧʽΪ
��2���Ҽ��ȷֽ�Ļ�ѧ����ʽΪ
��3����������ϡ�����У��������������壬�÷�Ӧ�����ӷ���ʽΪ
��4�������ʵ�鷽����֤��ʪ�ļ�¶���ڿ������Ƿ���ʣ�
���㣺������ƶ�
ר�⣺�ƶ���
������XY2����������ЧӦ����Ҫ���壬����Ϊ������̼����XΪC��YΪO�����ΪFeCO3����ΪFeC2O4����ʪ�ļ��ڿ�����ˮ�⣬���ɰ�ɫ����D��XY2��D�ڿ�����Ѹ�ٱ�ɻ���ɫ�����ձ�ɺ��ɫ����DΪFe��OH��2���Դ������
���
�⣺XY2����������ЧӦ����Ҫ���壬����Ϊ������̼����XΪC��YΪO�����ΪFeCO3����ΪFeC2O4����ʪ�ļ��ڿ�����ˮ�⣬���ɰ�ɫ����D��XY2��D�ڿ�����Ѹ�ٱ�ɻ���ɫ�����ձ�ɺ��ɫ����DΪFe��OH��2��
��1��������������֪��DΪFe��OH��2���Ļ�ѧʽΪFeCO3���ʴ�Ϊ��Fe��OH��2��FeCO3��
��2���Ҽ��ȷֽ�Ļ�ѧ����ʽΪFeC2O4
FeO+CO2��+CO�����ʴ�Ϊ��FeC2O4
FeO+CO2��+CO����
��3��������ϡ�����У��������������壬����ΪNO�Ͷ�����̼���÷�Ӧ�����ӷ���ʽΪ3FeCO3+10H++NO3-=3Fe3++NO��+3CO2��+5H2O��
�ʴ�Ϊ��3FeCO3+10H++NO3-=3Fe3++NO��+3CO2��+5H2O��
��4����ʪ�ļ�¶���ڿ����������ʻ��������ӣ���ȡ�����������ᣬ�ټ�SCN��Һ���ɫ������ʣ���֮����ɫ˵��û�б��ʣ��ʴ�Ϊ��ȡ�����������ᣬ�ټ�SCN��Һ���ɫ������ʣ���֮����ɫ˵��û�б��ʣ�
��1��������������֪��DΪFe��OH��2���Ļ�ѧʽΪFeCO3���ʴ�Ϊ��Fe��OH��2��FeCO3��
��2���Ҽ��ȷֽ�Ļ�ѧ����ʽΪFeC2O4
| ||
| ||
��3��������ϡ�����У��������������壬����ΪNO�Ͷ�����̼���÷�Ӧ�����ӷ���ʽΪ3FeCO3+10H++NO3-=3Fe3++NO��+3CO2��+5H2O��
�ʴ�Ϊ��3FeCO3+10H++NO3-=3Fe3++NO��+3CO2��+5H2O��
��4����ʪ�ļ�¶���ڿ����������ʻ��������ӣ���ȡ�����������ᣬ�ټ�SCN��Һ���ɫ������ʣ���֮����ɫ˵��û�б��ʣ��ʴ�Ϊ��ȡ�����������ᣬ�ټ�SCN��Һ���ɫ������ʣ���֮����ɫ˵��û�б��ʣ�
���������⿼��������ƶϣ�Ϊ��Ƶ���㣬���ա�XY2����������ЧӦ����Ҫ���塱����D�ڿ�����Ѹ�ٱ�ɻ���ɫ�����ձ�ɺ��ɫ��Ϊ����ͻ�ƿڣ����������仯����ת����������ԭ��Ӧ�Ŀ��飬��Ŀ�ѶȲ���

��ϰ��ϵ�д�
�����Ŀ
����˵����ȷ���ǣ�������
| A�����ࡢ��֬����������ȫȼ��ֻ����CO2 ��H2O |
| B�����飨C4H10���Ͷ��ȼ��鶼����ͬ���칹�� |
| C������ˮ�м��뱽�����ú�۲��²㼸����ɫ |
| D�����͡����͡�ֲ���Ͷ���̼�⻯���� |
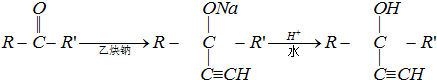
 ��̼̼˫������һ�������������������ã��磺
��̼̼˫������һ�������������������ã��磺
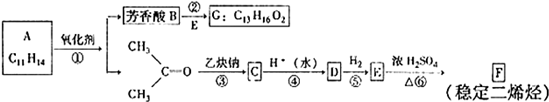
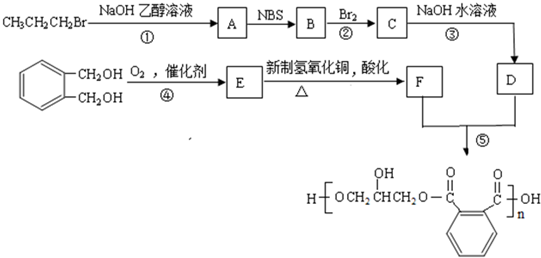
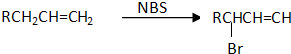
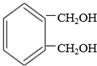 ��Ϊͬ���칹��Ľṹ��ʽ
��Ϊͬ���칹��Ľṹ��ʽ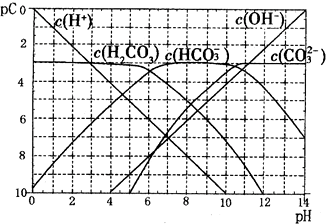
 ��һ�������¿�ʵ��ͼ��ʾ����֮��ı仯�����мס��ҡ������������ʾ���ʣ�������ĸ��ʾ�����
��һ�������¿�ʵ��ͼ��ʾ����֮��ı仯�����мס��ҡ������������ʾ���ʣ�������ĸ��ʾ�����