题目内容
下列各物质之间相互转化关系如下:
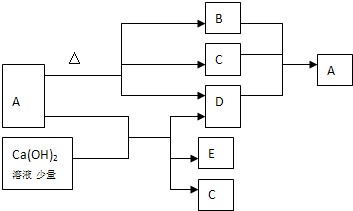
已知:A、B、C、D、E都是中学中常见化学物质,A 和D含有相同的金属阳离子,B为无色无味的气体,C是常见的无色液体,E是不溶于水的白色固体.请回答下列问题:
(1)写出A的化学式为: ,B的化学式: .
(2)写出B,C,D反应生成A的化学方程式: .
(3)检验A 和D阳离子的方法 (填名称).
(4)写出少量A 与过量Ca(OH)2溶液反应的离子方程式: .

已知:A、B、C、D、E都是中学中常见化学物质,A 和D含有相同的金属阳离子,B为无色无味的气体,C是常见的无色液体,E是不溶于水的白色固体.请回答下列问题:
(1)写出A的化学式为:
(2)写出B,C,D反应生成A的化学方程式:
(3)检验A 和D阳离子的方法
(4)写出少量A 与过量Ca(OH)2溶液反应的离子方程式:
考点:无机物的推断
专题:推断题
分析:A 和D含有相同的金属阳离子,B为无色无味的气体,C是常见的无色液体,E是不溶于水的白色固体,能和氢氧化钙反应生成白色沉淀说明A中含有碳酸根离子或碳酸氢根离子,因为碳酸盐在加热时不分解,则A是碳酸氢盐,则B是CO2、C是H2O,A能和氢氧化钙溶液反应生成碳酸钙、碳酸盐和水,A、B、C、D、E都是中学中常见化学物质,加热A易分解,则A是NaHCO3,D是Na2CO3,再结合题目分析解答.
解答:
解:A 和D含有相同的金属阳离子,B为无色无味的气体,C是常见的无色液体,E是不溶于水的白色固体,能和氢氧化钙反应生成白色沉淀说明A中含有碳酸根离子或碳酸氢根离子,因为碳酸盐在加热时不分解,则A是碳酸氢盐,则B是CO2、C是H2O,A能和氢氧化钙溶液反应生成碳酸钙、碳酸盐和水,A、B、C、D、E都是中学中常见化学物质,加热A易分解,则A是NaHCO3,D是Na2CO3,
(1)通过以上分析知,A是NaHCO3,B是CO2,故答案为:NaHCO3;CO2;
(2)向碳酸钠溶液中通入过量二氧化碳,发生反应为Na2CO3+H2O+CO2=2NaHCO3,故答案为:Na2CO3+H2O+CO2=2NaHCO3;
(3)A和D中都含有钠元素,可以采用焰色反应检验,故答案为:焰色反应;
(4)少量A 与过量Ca(OH)2溶液反应生成碳酸钙、氢氧化钠和水,离子方程式为HCO3-+Ca2++OH-=CaCO3↓+H2O,故答案为:HCO3-+Ca2++OH-=CaCO3↓+H2O.
(1)通过以上分析知,A是NaHCO3,B是CO2,故答案为:NaHCO3;CO2;
(2)向碳酸钠溶液中通入过量二氧化碳,发生反应为Na2CO3+H2O+CO2=2NaHCO3,故答案为:Na2CO3+H2O+CO2=2NaHCO3;
(3)A和D中都含有钠元素,可以采用焰色反应检验,故答案为:焰色反应;
(4)少量A 与过量Ca(OH)2溶液反应生成碳酸钙、氢氧化钠和水,离子方程式为HCO3-+Ca2++OH-=CaCO3↓+H2O,故答案为:HCO3-+Ca2++OH-=CaCO3↓+H2O.
点评:本题考查了无机物推断,根据物质的性质结合物质之间的反应、物质的颜色、状态进行推断,熟悉常见物质的性质是解本题关键,熟练掌握元素化合物知识并灵活运用这些知识解答,知道常见物质的检验方法,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列反应属于吸热反应的是( )
| A、稀硫酸与氢氧化钾溶液反应 |
| B、氢氧化钡晶体与氯化铵晶体研磨搅拌的反应 |
| C、锌与稀硫酸的反应 |
| D、生石灰变成熟石灰的反应 |
下列说法不正确的是( )
| A、在有盐桥构成的铜-锌-稀硫酸原电池中,盐桥中的阳离子移向电池的锌极 |
| B、化学平衡的建立与途径无关,可以从正反应方向建立,也可以从逆反应方向建立 |
| C、可以借助分光度计采用比色的方法测定某反应的化学反应速率 |
| D、在FeCl3与过量的KI溶液充分反应后的溶液用CCl4萃取后,往上层溶液中加入几滴KSCN溶液,溶液出现血红色,说明该化学反应存在限度 |
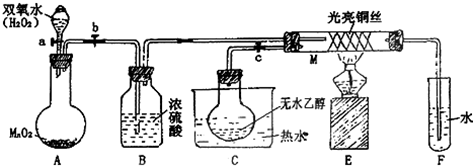
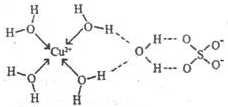 第四周期元素的单质及化合物在工农业生产中应用广泛.
第四周期元素的单质及化合物在工农业生产中应用广泛.