��Ŀ����
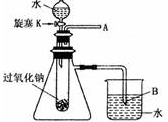 ����֬�ް�סԼ0.2g�������ƹ����ĩ������ʯ�����ϣ�Ȼ������й������Ƶ�λ�õμӼ���ˮ�������֬����ȼ��������
����֬�ް�סԼ0.2g�������ƹ����ĩ������ʯ�����ϣ�Ȼ������й������Ƶ�λ�õμӼ���ˮ�������֬����ȼ��������������������⣺
��1��д������������ˮ��Ӧ�Ļ�ѧ����ʽ
��2�������֬����ȼ�յ�ʵ����ʵ��ȼ�յ��������Եó��Ľ�����
��3��ij�о���ѧϰС�飬Ϊ��һ��֤���������ۣ�������ͼ��ʾ��װ�ý����й�ʵ�飮��д���йص�ʵ���������
����A����
���㣺ʵ��װ���ۺ�,�Ƶ���Ҫ������
ר�⣺ʵ����
��������1������������ˮ��Ӧ�����������ƺ�������
��2����������ȼ�յ�������֪����֬����ȼ�գ�˵���÷�Ӧ�Ƿ��ȷ�Ӧ���ҷ�Ӧ������ȼ���������ɣ����ó��Ľ����ǹ���������ˮ��Ӧ�ų�����������ȼ����ų���
��3�������һ��֤���������ۣ�����Ҫ��Kʹˮ��������Ʒ�Ӧ����������ͬʱ��A����һ�����ǵ�ľ�����ɣ�
��2����������ȼ�յ�������֪����֬����ȼ�գ�˵���÷�Ӧ�Ƿ��ȷ�Ӧ���ҷ�Ӧ������ȼ���������ɣ����ó��Ľ����ǹ���������ˮ��Ӧ�ų�����������ȼ����ų���
��3�������һ��֤���������ۣ�����Ҫ��Kʹˮ��������Ʒ�Ӧ����������ͬʱ��A����һ�����ǵ�ľ�����ɣ�
���
�⣺��1������������ˮ��Ӧ�����������ƺ���������Ӧ�Ļ�ѧ����ʽ2Na2O2+2H2O=4NaOH+O2�����ʴ�Ϊ��2Na2O2+2H2O=4NaOH+O2����
��2����֬����ȼ�գ�˵���÷�Ӧ�Ƿ��ȷ�Ӧ���ҷ�Ӧ������ȼ���������ɣ���ʵ�����Ϊ����������ˮ��Ӧ�ų�����������ȼ����ų���
�ʴ�Ϊ������������ˮ��Ӧ�ų�����������ȼ����ų���
��3����һ��֤���������ۣ���ʵ�����Ϊ��A������A����һ�����ǵ�ľ�����۲쵽A�������ǵ�ľ����ȼ��B�������ݷų������������ۺ�����
�ʴ�Ϊ����A������A����һ�����ǵ�ľ���������ǵ�ľ����ȼ�������ݷų���
��2����֬����ȼ�գ�˵���÷�Ӧ�Ƿ��ȷ�Ӧ���ҷ�Ӧ������ȼ���������ɣ���ʵ�����Ϊ����������ˮ��Ӧ�ų�����������ȼ����ų���
�ʴ�Ϊ������������ˮ��Ӧ�ų�����������ȼ����ų���
��3����һ��֤���������ۣ���ʵ�����Ϊ��A������A����һ�����ǵ�ľ�����۲쵽A�������ǵ�ľ����ȼ��B�������ݷų������������ۺ�����
�ʴ�Ϊ����A������A����һ�����ǵ�ľ���������ǵ�ľ����ȼ�������ݷų���
���������⿼�������ƺ�ˮ���й�ʵ��̽�����������е��Ѷȵ����⣬���������ǿ������ʵ��������������ѵ������������Ҫ��ѧ���������桢ϸ�µ����⣬��ϵ��ѧ����֪ʶ�ͼ��ܣ�����֪ʶ����ȡ�Ǩ�ơ����飬ȫ��ϸ�µ�˼�����ܵó���ȷ�Ľ��ۣ�����������ѧ���������⡢��������������

��ϰ��ϵ�д�
�����Ŀ
25�棬101k Paʱ��ǿ����ǿ���ϡ��Һ�����кͷ�Ӧ���к���Ϊ-57.3kJ?mol-1������ı�ȼ����Ϊ-5518kJ?mol-1�������Ȼ�ѧ����ʽ��д��ȷ���ǣ�������
| A��2H+��aq��+SO42- ��aq��+Ba2+��aq��+2OH-��aq��=BaSO4��s��+2H2O��l����H=-114.6 kJ?mol-1 | ||
| B��2KOH��aq��+H2SO4��aq��=K2SO4��aq��+2H2O��l����H=-57.3 kJ?mol-1 | ||
C��C8H18��1��+
| ||
D��C8H18��g��+
|
���Ĵ�����4NH3��g��+5O2��g��?4NO��g��+6H2O��g����H=-1025kJ?mol-1�ǹ�ҵ�Ʊ��������Ҫ��Ӧ��һ�������½�4mol NH3��5mol O2��ϲ�ͨ��̶��ݻ�Ϊ2L���ܱ������У���10s�÷�Ӧ��ƽ�⣬�����NO��Ũ��Ϊ0.8mol?L-1�������ж���ȷ���ǣ�������
| A����O2Ũ�ȱ仯��ʾ�ķ�Ӧ����Ϊ0.064 mol?��L?s��-1 | ||
| B����Ӧ�ﵽƽ��״̬ʱNH3��ת����Ϊ20% | ||
C�������¶���ʹ
| ||
| D���������������Ϊ4 L��ƽ��ʱNO��Ũ��С��0.4 mol?L-1 |