题目内容
8.如图是部分短周期元素化合价与原子序数的关系图,下列说法不正确的是( )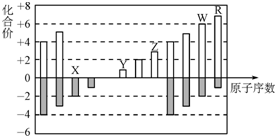
| A. | 离子半径:X>Y>Z | |
| B. | WX3和水反应形成的化合物是离子化合物 | |
| C. | 最高价氧化物对应的水化物酸性:R>W | |
| D. | Y和Z两者最高价氧化物对应的水化物能相互反应 |
分析 这几种元素都是短周期元素,根据元素化合价知,X是O元素、Y是Na元素、Z是Al元素、W是S元素、R是Cl元素;
A.X、Y、Z离子的电子层结构相同,电子层结构相同的离子,离子半径随着原子序数增大而减小;
B.SO3和水反应形成的化合物是H2SO4,硫酸分子中只含共价键;
C.同一周期元素,元素的非金属性随着原子序数增大而增强,元素的非金属性越强,其最高价氧化物的水化物酸性越强;
D.Y、Z两者的最高价氧化物对应的水化物分别是NaOH、Al(OH)3,氢氧化铝属于两性氢氧化物,能溶于强酸强碱溶液.
解答 解:这几种元素都是短周期元素,根据元素化合价知,X是O元素、Y是Na元素、Z是Al元素、W是S元素、R是Cl元素;
A.X、Y、Z离子的电子层结构相同,电子层结构相同的离子,离子半径随着原子序数增大而减小,原子序数X<Y<Z,则离子半径X>Y>Z,故A正确;
B.SO3和水反应形成的化合物是H2SO4,硫酸分子中只含共价键,为共价化合物,故B错误;
C.同一周期元素,元素的非金属性随着原子序数增大而增强,元素的非金属性越强,其最高价氧化物的水化物酸性越强,非金属性W<R,则最高价氧化物对应的水化物酸性:R>W,故C正确;
D.Y、Z两者的最高价氧化物对应的水化物分别是NaOH、Al(OH)3,氢氧化铝属于两性氢氧化物,能溶于强酸强碱溶液,NaOH是强碱,所以Y、Z两者的最高价氧化物对应的水化物能相互反应,故D正确;
故选B.
点评 本题考查原子结构和元素性质,为高频考点,侧重考查学生分析判断及对知识的灵活运用,明确原子结构、元素周期表结构、元素周期律、物质性质是解本题关键,注意离子半径大小比较方法,题目难度不大.

练习册系列答案
相关题目
18.NA为阿伏加德罗常数,下列描述正确的是( )
| A. | 含有NA个氦原子的氦气在标准状况下的体积约为11.2L | |
| B. | 40 g NaOH溶解在1 L水中,所制得的溶液,物质的量浓度为1 mol•L-1 | |
| C. | 标准状况下,11.2 L四氯化碳所含分子数为0.5NA | |
| D. | 常温常压下,5.6g铁与过量的盐酸反应转移电子总数为0.2NA |
19.除去下列物质中所含的杂质(括号内为杂质),选用试剂正确的是( )
| A. | FeCl2溶液(FeCl3):Fe粉 | B. | CO2(SO2):饱和的Na2CO3溶液 | ||
| C. | SO2(HCl):NaOH溶液 | D. | NaHCO3溶液(Na2CO3):Ca(OH)2溶液 |
16. “黑索金”是一种烈性炸药.“黑索金”是由乌洛托品(分子结构如图)与发烟硝酸作用制得.下列说法中不正确的是( )
“黑索金”是一种烈性炸药.“黑索金”是由乌洛托品(分子结构如图)与发烟硝酸作用制得.下列说法中不正确的是( )
 “黑索金”是一种烈性炸药.“黑索金”是由乌洛托品(分子结构如图)与发烟硝酸作用制得.下列说法中不正确的是( )
“黑索金”是一种烈性炸药.“黑索金”是由乌洛托品(分子结构如图)与发烟硝酸作用制得.下列说法中不正确的是( )| A. | 乌洛托品中碳原子均达到饱和结构 | |
| B. | 乌洛托品的一氯代物只有一种 | |
| C. | 乌洛托品的分子式为C6H12N4 | |
| D. | 乌洛托品分子结构中含有3个六元环 |
3.能源可划分为一级能源和二级能源.自然界中以现成形式提供的能源为一级能源;需依靠 其他能源的能量间接制取的能源为二级能源.下列叙述正确的是( )
| A. | 电能是一级能源 | B. | 水煤气是二级能源 | ||
| C. | 天然气是二级能源 | D. | 水能是二级能源 |
13.X、Y、Z、M、N是元素周期表中的短周期主族元素,且原子序数依次递增.已知X的最外 层电子数是次外层电子数的3倍,X、M同主族,Y在同周期主族元素中原子半径最大.Z和N可以形成ZN2型化合物.下列有关说法正确的是( )
| A. | X 与 Y 只能形成一种化合物 | |
| B. | 单质的氧化性:X<M | |
| C. | 气态氢化物的稳定性:M>N | |
| D. | 最高价氧化物对应水化物的碱性:Y>Z |