题目内容
水的电离过程为H2O?H++OH-,在不同温度下,其离子积分别为KW(25℃)=1.0×10-14 mol2?L-2,KW(35℃)=2.1×10-14 mol2?L-2,则下列叙述正确的是( )
| A、[H+]随着温度的升高而降低 |
| B、在35℃时,[H+]>[OH-] |
| C、水的电离程度 α(25℃)>α(35℃) |
| D、[OH-]随温度升高而增大 |
考点:水的电离
专题:电离平衡与溶液的pH专题
分析:水中存在电离平衡,电离过程是吸热过程,温度升高促进电离,氢离子浓度和氢氧根离子浓度增大;水中氢离子浓度始终等于氢氧根离子浓度,水是中性,据此进行解答.
解答:
解:A、水的电离为吸热过程,温度升高促进水的电离,氢离子浓度增大,故A错误;
B、在35℃时,水电离出的氢离子浓度、氢氧根离子浓度比25°C大,但水为中性,则[H+]=[OH-],故B错误;
C、升温促进水的电离程度,水的电离度增大,所以水的电离度:α(25℃)<α(35℃),故C错误;
D、水的电离是吸热过程,升高温度后水电离的氢离子、氢氧根离子浓度都增大,故D正确;
故选D.
B、在35℃时,水电离出的氢离子浓度、氢氧根离子浓度比25°C大,但水为中性,则[H+]=[OH-],故B错误;
C、升温促进水的电离程度,水的电离度增大,所以水的电离度:α(25℃)<α(35℃),故C错误;
D、水的电离是吸热过程,升高温度后水电离的氢离子、氢氧根离子浓度都增大,故D正确;
故选D.
点评:本题考查了水的电离及其影响,题目难度不大,注意掌握温度、溶液酸碱性对水的电离的影响,选项B为易错点,需要明确35℃时的KW大于25℃时的KW,说明升高温度水的电离平衡右移,[H+]、[OH-]都增大,但是仍相等.

练习册系列答案
 精英口算卡系列答案
精英口算卡系列答案 应用题点拨系列答案
应用题点拨系列答案 状元及第系列答案
状元及第系列答案 同步奥数系列答案
同步奥数系列答案
相关题目
已知2SO2(g)+O2(g)?2SO3(g);△H=-197kJ?mol-1.向同温、同体积的三个密闭容器中分别充入气体:(甲)2mol SO2和1mol O2;(乙)1mol SO2和0.5mol O2;(丙)2mol SO3.恒温、恒容下反应达平衡时,下列关系一定正确的是( )
| A、容器内压强P:P甲=P丙>2P乙 |
| B、SO3的质量m:m甲=m丙>2m乙 |
| C、平衡常数:K甲=K丙=K乙 |
| D、反应放出或吸收热量的数值Q:Q甲+Q丙>197kJ |
(双项)下列说法中,正确的是( )
| A、烃基与羧基直接相连的化合物叫做羧酸 |
| B、饱和链状羧酸的组成符合CnH2nO2 |
| C、羧酸在常温下都能发生酯化反应 |
| D、羧酸的官能团是-COOH |
光导纤维是一种现代化的通讯工具,制造光导纤维的主要原料是( )
| A、纯硅 |
| B、CaO |
| C、纯SiO2 |
| D、沙子 |
海水是重要的资源,可以制备一系列物质如图.下列说法正确的是( )
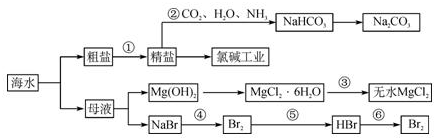

| A、步骤④、⑤、⑥反应中,溴元素均被氧化 | ||
B、除去粗盐中的S
| ||
| C、步骤②中,应先通CO2,再通NH3 | ||
| D、步骤③可将MgCl2?6H2O晶体在空气中直接加热脱水 |
在我国文明发展过程中,最早较广泛使用的金属是( )
| A、铜 | B、铁 | C、铝 | D、铅 |
下列叙述中正确的是( )
| A、第三周期元素的离子半径从左到右依次减小 |
| B、HCl、PCl3、N2、CO2分子中所有原子都满足最外层8电子的结构 |
| C、晶体内可以不存在化学键,也可以同时存在离子键、极性键和非极性键 |
| D、若某离子化合物X2Y3中X3+和Y2-的电子层结构相同,则X、Y两元素的原子序数之差一定为6 |