题目内容
已知:H2(g) + F2(g) = 2HF(g) ΔH=? 270 kJ/mol,下列说法正确的是
- A.在相同条件下,1 mol H2与1 mol F2的能量总和大于2 mol HF气体的能量
- B.1 mol H2与1 mol F2反应生成2 mol液态HF放出的热量小于270 kJ
- C.该反应的逆反应是放热反应
- D.
该反应过程的能量变化可用下图来表示
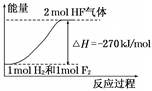
A
试题分析:A、ΔH=E生-E反?0 E生?E反,所以反应物:1 mol H2与1 mol F2的能量大于生成物:2 mol HF的能量,正确;B、2 mol液态HF的能量低于2 mol HF气体的能量,放出的热量大于270 kJ,错误;C、该反应的逆反应是吸热反应,错误;D、反应物:1 mol H2与1 mol F2的能量大于生成物:2 mol HF的能量, 错误。
考点:考查化学反应与能量等相关知识。
试题分析:A、ΔH=E生-E反?0 E生?E反,所以反应物:1 mol H2与1 mol F2的能量大于生成物:2 mol HF的能量,正确;B、2 mol液态HF的能量低于2 mol HF气体的能量,放出的热量大于270 kJ,错误;C、该反应的逆反应是吸热反应,错误;D、反应物:1 mol H2与1 mol F2的能量大于生成物:2 mol HF的能量, 错误。
考点:考查化学反应与能量等相关知识。

练习册系列答案
 学期复习一本通学习总动员期末加暑假延边人民出版社系列答案
学期复习一本通学习总动员期末加暑假延边人民出版社系列答案 芒果教辅暑假天地重庆出版社系列答案
芒果教辅暑假天地重庆出版社系列答案
相关题目
已知:H2(g)
+I2(g)  2HI(g) ΔH = -14.9 kJ/mol。在甲、乙两个体积相同密闭容器中充入反应物,保持恒温恒容,其起始浓度如下表所示。甲中反应达到平衡时,测得c(H2)=0.008 mol/L。
下列判断正确的
2HI(g) ΔH = -14.9 kJ/mol。在甲、乙两个体积相同密闭容器中充入反应物,保持恒温恒容,其起始浓度如下表所示。甲中反应达到平衡时,测得c(H2)=0.008 mol/L。
下列判断正确的
|
起始浓度 |
c(H2) / mol/L |
c(I2) / mol/L |
c(HI) / mol/L |
|
甲 |
0.01 |
0.01 |
0 |
|
乙 |
0.02 |
0.02 |
0 |
A.平衡时,乙中H2的转化率是甲中的2倍
B.平衡时,甲中混合物的颜色比乙中深
C.平衡时,甲、乙中热量的变化值相等
D.该温度下,反应的平衡常数K=0.25