题目内容
下列关于盐酸与醋酸两种溶液的说法正确的是( )
| A、pH相同的两溶液浓度相同 |
| B、中和等物质的量的氢氧化钠消耗的两种酸的物质的量相同 |
| C、pH相同的两溶液稀释10倍后,pH不相同 |
| D、pH=3的两溶液加入等体积的pH=3的硫酸,两溶液中c(H+)都不变 |
考点:弱电解质在水溶液中的电离平衡
专题:电离平衡与溶液的pH专题
分析:盐酸是强酸,在溶液中完全电离,醋酸是弱酸,不能完全电离,加水稀释会促进电离,据此回答.
解答:
解:A、pH相同的两溶液浓度不相同,醋酸浓度大,故A错误;
B、两种酸和氢氧化钠都是等物质的量反应,中和等物质的量的氢氧化钠消耗的两种酸的物质的量相同,故B正确;
C、pH相同的两溶液稀释10倍后,pH不相同,醋酸的较小,因为会促进醋酸的电离,故C正确;
D、pH=3的两溶液加入等体积的pH=3的硫酸,HCl是完全电离的,但是硫酸抑制醋酸的电离,所以醋酸的c(H+)会比盐酸的小,故D错误.
故选BC.
B、两种酸和氢氧化钠都是等物质的量反应,中和等物质的量的氢氧化钠消耗的两种酸的物质的量相同,故B正确;
C、pH相同的两溶液稀释10倍后,pH不相同,醋酸的较小,因为会促进醋酸的电离,故C正确;
D、pH=3的两溶液加入等体积的pH=3的硫酸,HCl是完全电离的,但是硫酸抑制醋酸的电离,所以醋酸的c(H+)会比盐酸的小,故D错误.
故选BC.
点评:本题是一道关于弱电解质的稀释和电离平衡的移动等知识,注意强酸和弱酸的电离程度的区别是关键,难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列说法中正确的是( )
| A、价电子为ns2的元素肯定为金属元素 |
| B、同一原子中不可能有两个运动状态完全相同的电子 |
| C、同一主族元素形成的氧化物的晶体类型相同 |
| D、同一原子中不可能有两个能量相同的轨道 |
下列溶液中,与100ml 0.5mol/L NaCl溶液所含的Cl-的物质的量浓度相同的是( )
| A、100 mL 0.5 mol/L MgCl2 溶液 |
| B、200 mL 0.25 mol/L HCl溶液 |
| C、50 mL 0.5 mol/L KClO3溶液 |
| D、200 mL 0.25 mol/L CaCl2溶液 |
下列反应的离子方程式书写正确的是( )
| A、硫酸铝溶液中加入过量氨水Al3++3OH-═Al(OH)3↓ | ||||
| B、碳酸钙与醋酸反应CaCO3+2H+═Ca2++CO2↑+H2O | ||||
| C、硫酸亚铁溶液中加入用硫酸酸化的过氧化氢溶液Fe2++2H++H2O2═Fe3++2H2O | ||||
D、电解饱和食盐水2Cl-+2H2O
|
下列物质分类正确的是( )
| A、SO2、SiO2、CO均为酸性氧化物 |
| B、稀豆浆、肥皂水、氯化铁溶液均为胶体 |
| C、烧碱、硫酸、乙醇均为电解质 |
| D、盐酸、水玻璃、氨水均为混合物 |
 如图:是一套实验室制气装置,用于发生、干燥、收集和吸收有毒气体.下列各组物质能利用这套装置进行实验的是( )
如图:是一套实验室制气装置,用于发生、干燥、收集和吸收有毒气体.下列各组物质能利用这套装置进行实验的是( )| A、电石和水 |
| B、MnO2和浓盐酸 |
| C、Cu片和浓硝酸 |
| D、Na2SO3(s)和浓硫酸 |
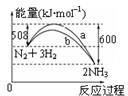 根据下列叙述写出相应的热化学方程式:
根据下列叙述写出相应的热化学方程式: