题目内容
9.防治酸雨首先要从消除污染源着手,可开发氢能、太阳能、核能等替代化合燃料,从根本上防止酸雨的产生.其次可利用各种物理及化学方法.(1)钙基固硫:在煤中添加生石灰(或石灰石),该法还可变废为宝,得到CaSO4.发生反应的化学方程式有①SO2+CaO$\frac{\underline{\;高温\;}}{\;}$CaSO3,②2CaSO3+O2$\frac{\underline{\;高温\;}}{\;}$CaSO4;
(2)氨水吸收:将含SO2的工业尾气用氨水吸收,吸收液再用硫酸处理,得到高纯度SO2和一种氮肥,发生反应的化学方程式有①2NH3+H2O+SO2═(NH4)2SO3,②(NH4)2SO3+H2SO4═(NH4)2SO4+SO2↑+H2O;
(3)Na2SO3吸收:将SO2用Na2SO3吸收,再加热所得固体,该法可循环使用Na2SO3.发生反应的化学方程式有①Na2SO3+SO2+H2O=2NaHSO3,②2NaHSO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2SO3+SO2↑+H2O.
分析 (1)氧化钙与硫反应生成亚硫酸钙,亚硫酸钙与氧气在高温下反应生成硫酸钙;
(2)氨气与二氧化硫反应生成亚硫酸铵,亚硫酸铵与硫酸反应生成硫酸铵、二氧化硫气体和水;
(3)二氧化硫与亚硫酸钠反应生成亚硫酸氢钠,加热亚硫酸氢钠分解得到亚硫酸钠、二氧化硫气体和水,据此写出反应的化学方程式.
解答 解:(1)在煤中添加生石灰(或石灰石),该法还可变废为宝,得到CaSO4,反应的化学方程式分别为:SO2+CaO$\frac{\underline{\;高温\;}}{\;}$CaSO3、②2CaSO3+O2$\frac{\underline{\;高温\;}}{\;}$CaSO4,
故答案为:SO2+CaO$\frac{\underline{\;高温\;}}{\;}$CaSO3;2CaSO3+O2$\frac{\underline{\;高温\;}}{\;}$CaSO4;
(2)将含SO2的工业尾气用氨水吸收,吸收液再用硫酸处理,得到高纯度SO2和一种氮肥,该氮肥为硫酸铵,反应的化学方程式分别为:2NH3+H2O+SO2═(NH4)2SO3、(NH4)2SO3+H2SO4=═(NH4)2SO4+SO2↑+H2O,
故答案为:2NH3+H2O+SO2═(NH4)2SO3;(NH4)2SO3+H2SO4═(NH4)2SO4+SO2↑+H2O;
(3)将SO2用Na2SO3吸收,再加热所得固体亚硫酸钠、二氧化硫气体和水,该法可循环使用Na2SO3,反应的化学方程式为:Na2SO3+SO2+H2O=2NaHSO3、2NaHSO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2SO3+SO2↑+H2O,
故答案为:Na2SO3+SO2+H2O=2NaHSO3;2NaHSO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2SO3+SO2↑+H2O.
点评 本题考查了化学方程式的书写,题目难度中等,明确反应实质为解答关键,注意掌握化学方程式的书写原则,试题培养了学生的分析能力及灵活应用能力.

| A. | 用溴水鉴别苯、乙醇、苯乙烯 | |
| B. | 苯、溴水、铁粉混合制溴苯 | |
| C. | 用分液漏斗分离苯和乙醇 | |
| D. | 加浓溴水,然后过滤除去苯中混有的少量己烯 |
| A. | CCl4和SiCl4的熔点 | |
| B. | 邻羟基苯甲醛( )和对羟基苯甲醛( )和对羟基苯甲醛(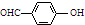 )的沸点 )的沸点 | |
| C. | HF和HCl在水中的溶解度 | |
| D. | H2SO3和H2SO4的酸性 |
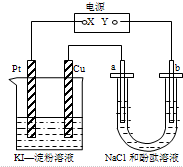
| A. | X可以是电源的负极,也可以是电源的正极 | |
| B. | 甲装置的电池反应是:2Cu2++4I-=2CuI↓+I2 | |
| C. | 乙装置a电极周围溶液变红色,pH变大 | |
| D. | 乙装置中Na+向b电极迁移 |
| A. | 苯甲醇 | B. | 2-丙醇 | ||
| C. | 2,2-二甲基-1-丙醇 | D. | 2-甲基-2-丙醇 |
 元素周期表是学习化学的重要工具,右图是元素周期表中的一格,以下获取的信息错误的是( )
元素周期表是学习化学的重要工具,右图是元素周期表中的一格,以下获取的信息错误的是( )| A. | 该元素的原子序数是53 | B. | 该元素属于金属元素 | ||
| C. | 该元素的原子核外有53个电子 | D. | 该元素的相对原子质量为126.9 |
| A. | 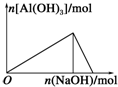 向AlCl3溶液中滴加NaOH溶液 | B. | 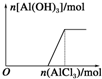 向NaOH溶液中滴加AlCl3溶液 | ||
| C. | 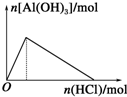 向Na[Al(OH)4]溶液中通入CO2 | D. |  向AlCl3溶液中滴氨水 |
| A. | 铁与稀硫酸反应:Fe+2H+═Fe3++H2↑ | |
| B. | 氢氧化铝与足量盐酸反应:Al(OH)3+3H+═Al3++3H2O | |
| C. | 钠和冷水反应:Na+2H2O═Na++H2↑+OH- | |
| D. | 过量二氧化碳与苛性钾反应:CO2+2OH-═CO32-+H2O |