题目内容
下列离子方程式正确的是
A.醋酸除去水垢中的CaCO3:CaCO3+2H+=Ca2++H2O+CO2↑
B.碘水中通入足量的SO2:I2 +SO2+2H2O=2HI+SO42-+2H+
C.NaHSO4溶液与Ba(OH)2溶液反应至中性:H++SO42-+Ba2++OH-=BaSO4↓+H2O
D.4mol·L-1的NaAlO2溶液和7 mol·L-1的盐酸溶液等体积混合均匀4AlO2-+7H++H2O=3A1(OH)3↓+Al3+
D
【解析】
试题分析:A. 醋酸是弱酸,应该写化学式,醋酸除去水垢中的CaCO3的离子方程式是:CaCO3+2CH3COOH =Ca2++2CH3COO-+H2O+CO2↑,错误;B.HI是强酸,完全电离,二者反应的离子方程式是:I2 +SO2+ 2H2O=2I-+SO42-+4H+,错误;C.NaHSO4溶液与Ba(OH)2溶液反应至中性:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O,错误;D.4 mol·L-1的NaAlO2溶液和7 mol·L-1的盐酸溶液等体积混合均匀,由于n(AlO2-):n(H+)=4:7,所以反应的离子方程式是:4AlO2-+7H++H2O=3A1(OH)3↓+Al3+,正确。
考点:考查离子方程式书写的正误判断的知识。

练习册系列答案
 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案
相关题目

 2CO2 (g) +N2 (g)
2CO2 (g) +N2 (g) 
 =-867kJ·mol-1
=-867kJ·mol-1 N2O4(g)
N2O4(g) 
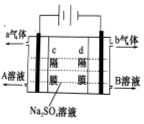
 2H2SO4+4NaOH+O2↑+2H2↑
2H2SO4+4NaOH+O2↑+2H2↑ 。下列有关咖啡酸的说法中,错误的是
。下列有关咖啡酸的说法中,错误的是
 R-CHO+R′-CHO;
R-CHO+R′-CHO;