题目内容
FeCl3溶液和Fe(OH)3胶体共同具备的性质是( )
| A、都不稳定,密封静置,会产生沉淀 |
| B、都能产生丁达尔现象 |
| C、分散质微粒都可以透过滤纸 |
| D、加入盐酸先产生沉淀,随后溶解 |
考点:胶体的重要性质
专题:
分析:A.溶液与胶体都是稳定的分散系;
B.丁达尔效应是胶体特有性质;
C.依据胶体、溶液中分散质粒度小于滤纸孔径解答;
D.氯化铁加入盐酸不会产出沉淀.
B.丁达尔效应是胶体特有性质;
C.依据胶体、溶液中分散质粒度小于滤纸孔径解答;
D.氯化铁加入盐酸不会产出沉淀.
解答:
解:A.溶液与胶体都是稳定的分散系,密封静置,不会产生沉淀,故A错误;
B.Fe(OH)3胶体具有丁达尔效应,氯化铁溶液不具有,故B错误;
C.胶体、溶液中分散质粒度小于滤纸孔径,都可以透过滤纸,故C正确;
D.Fe(OH)3胶体加入盐酸先产生沉淀,随后溶解,FeCl3溶液加入盐酸无现象,故D错误;
故选:C.
B.Fe(OH)3胶体具有丁达尔效应,氯化铁溶液不具有,故B错误;
C.胶体、溶液中分散质粒度小于滤纸孔径,都可以透过滤纸,故C正确;
D.Fe(OH)3胶体加入盐酸先产生沉淀,随后溶解,FeCl3溶液加入盐酸无现象,故D错误;
故选:C.
点评:本题考查了胶体的性质以及胶体和溶液的区别,明确胶体的性质是解题关键,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
NA代表阿伏加德罗常数,下列说法正确的是( )
| A、同一物质的固、液、气三种状态的熵相同 |
| B、0.1 mol铁在0.1 mol Cl2中充分燃烧,有0.3NA个电子转移 |
| C、等物质的量的钠分别在足量的氧气和氯气中燃烧,转移电子数相等 |
| D、1.5 mol NO2与足量H2O反应,转移的电子数为2NA |
甲、乙是周期表中同一主族的两种元素,若甲的原子序数为x,则乙的原子序数不可能是( )
| A、x+4 | B、x+8 |
| C、x+10 | D、x+18 |
下列反应的离子方程式书写正确的是( )
| A、向稀硫酸中加入铁片:2Fe+6H+=2Fe3++3H2↑ |
| B、向稀醋酸中加入碳酸钙:CaCO3+2H+=Ca2++H2O+CO2↑ |
| C、向氢氧化钡溶液中加入稀硫酸:H++OH-=H2O |
| D、向澄清石灰水中加入少量碳酸氢钠溶液:Ca2++OH-+HCO3-=CaCO3↓+H2O |
下列离子方程式书写正确的是( )
| A、氯气跟水反应:Cl2+H2O=2H++Cl-+ClO- |
| B、硫酸铜溶液跟氢氧化钡溶液反应:Ba2++SO42-=BaSO4↓ |
| C、碳酸钠溶液中加入少量稀盐酸:CO32-+H+=HCO3- |
| D、铜与稀盐酸反应:Cu+2H+=Cu2++H2↑ |
下列化合物中,属于盐的是( )
| A、H2O |
| B、Na2CO3 |
| C、HNO3 |
| D、KOH |
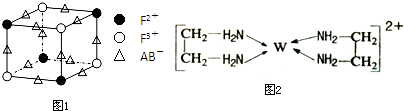 已知A、B、C、D、E、F、W都是周期表中前四周期的元素,它们的核电荷数依次增大,其中A、B、C、D、E为不同主族的元素.A、C的最外层电子数都是其电子层数的2倍,B的电负性大于C,透过蓝色钴玻璃观察E的焰色反应为紫色,F的基态原子中有4个未成对电子,W的+1价阳离子正好充满K,L,M三个电子层.回答下列问题:
已知A、B、C、D、E、F、W都是周期表中前四周期的元素,它们的核电荷数依次增大,其中A、B、C、D、E为不同主族的元素.A、C的最外层电子数都是其电子层数的2倍,B的电负性大于C,透过蓝色钴玻璃观察E的焰色反应为紫色,F的基态原子中有4个未成对电子,W的+1价阳离子正好充满K,L,M三个电子层.回答下列问题: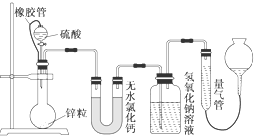 不同浓度的硫酸与锌反应时,硫酸可以被还原为SO2,也可被还原为氢气.某校研究性学习小组拟设计实验验证这一事实,并进行数据测定和相关计算.
不同浓度的硫酸与锌反应时,硫酸可以被还原为SO2,也可被还原为氢气.某校研究性学习小组拟设计实验验证这一事实,并进行数据测定和相关计算.