题目内容
11.设NA表示阿伏伽德罗常数的值,下列说法正确的是( )| A. | 1L 1mol/LNaAlO2溶液中含有氧原子数为2NA | |
| B. | 标准状况下,33.6L三氧化硫中含有硫原子的数目为1.5NA | |
| C. | 1mol(-14CD3)中所含的中子数和电子数分别为11NA、9NA | |
| D. | 精练铜的过程中,当阳极溶解32g铜时转移的电子数为NA |
分析 A.溶液中含有水;
B.标况下,三氧化硫为固体;
C.甲基(-14CD3)中含有11个中子、9个电子;
D.粗铜中含有杂质,电解过程中杂质铁、锌等优先放电,导致阳极溶解的铜减少.
解答 解:A.溶液中含有水,氧原子数大于2NA,故A错误;
B.标况下,三氧化硫为固体,不能根据气体摩尔体积来计算其物质的量,故B错误;
C.甲基(-14CD3)中含有11个中子、9个电子,1mol该甲基中含有11中子、9mol电子,故C正确;
D.电解精炼铜时每转移NA个电子,转移了1mol电子,由于粗铜中含有较活泼的杂质Fe、Zn等,电解时杂质优先放电,所以当阳极溶解32g铜时转移的电子数大于NA,故D错误.
故选C.
点评 本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
8.已知2H2O2(aq)=2H2O(l)+O2(g)△H=-196KJ•mol-1,常温下,往H2O2溶液中滴加少量FeCl2溶液,可发生如下两个反应:2Fe2++H2O2+2H+=2Fe3++2H2O,2Fe3++H2O2=2Fe2++O2↑+2H+下列有关反应的说法正确的是( )
| A. | 在H2O2分解过程中,溶液的pH逐渐下降 | |
| B. | Fe3+是该反应的催化剂 | |
| C. | 2H2O(l)+O2(g)=2H2O2(aq)在一定条件下能够自发进行 | |
| D. | v(H2O2)=2v(O2) |
2.在一定温度下,将气体X和气体Y各0.16mol充入10L恒容密闭容器中,发生反应:X(g)+Y(g)?2Z(g)△H<0.一段时间后达到平衡,反应过程中测定的数据如下表:下列说法正确的是( )
| t/min | 2 | 4 | 7 | 9 |
| n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
| A. | 反应前2 min的平均速率v(Z)=2.0×10-3mol•L-1•min-1 | |
| B. | 其他条件不变,降低温度,反应达到新平衡前v(逆)>v(正) | |
| C. | 保持其他条件不变,起始时向容器中充入0.32 mol气体X和0.32 mol气体Y,到达平衡时,n(Z)=0.24 mol | |
| D. | 其他条件不变,向平衡体系中再充入0.16 mol气体X,与原平衡相比,达到新平衡时,气体Y的转化率增大,X的体积分数增大 |
19.汽车安全气囊是汽车安全性辅助配置之一.汽车剧烈碰撞时,安全气囊中发生以下反应:NaN3+KNO3→K2O+Na2O+N2↑(未配平),则下列判断不正确的是( )
| A. | NaN3是还原剂 | |
| B. | 氧化产物与还原产物物质的量之比为1:15 | |
| C. | N2既是氧化产物又是还原产物 | |
| D. | 标准状况下,当有10mol电子转移时生成358.4L N2 |
6.在氯化铁、氯化铜和盐酸的混合溶液中加入过量铁粉,则反应后溶液中存在较多的阳离子是( )
| A. | Cu2+ | B. | Fe3+ | C. | Fe2+ | D. | H+ |
16.下列有机物同分异构体数目相同的是( )
| A. | 分子式为C4H8的烃与丙烷的二氯取代物 | |
| B. | 分子式为C5H12的烃与分子式为C2H4O2且能发生银镜反应的有机物 | |
| C. | 分子式都为C8H10O的醇和酚 | |
| D. | 甲苯的一氯取代物与分子式为C4H10O的醇 |
20.实验室要配制1.0mol/L硫酸溶液500mL,需要用10mol/L的硫酸溶液的体积是( )
| A. | 25mL | B. | 250mL | C. | 50mL | D. | 500mL |

 ,F中的含氧官能团名称酚羟基、羧基;
,F中的含氧官能团名称酚羟基、羧基; ;
; +2H2O.
+2H2O.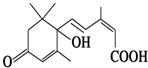 北京奥运会期间对大量盆栽鲜花施用了S诱抗素制剂,以保持鲜花盛开.S诱抗素的分子结构如图,根据S诱抗素结构,可知S诱抗素分子中含有的官能团有羰基、碳碳双键、羟基、羧基.
北京奥运会期间对大量盆栽鲜花施用了S诱抗素制剂,以保持鲜花盛开.S诱抗素的分子结构如图,根据S诱抗素结构,可知S诱抗素分子中含有的官能团有羰基、碳碳双键、羟基、羧基.