题目内容
如图中a、b、c、d、e、f为元素周期表中前4周期的一部分元素,下列有关叙述正确的是( )
| a | ||||
| b | c | |||
| d | e | |||
| f |
| A、b、c、e三种元素的原子半径大小关系:e>c>b |
| B、六种元素分别形成的单质固体中,d的熔、沸点最高 |
| C、c的氢化物沸点比f的氢化物沸点低 |
| D、b元素除0价外,只有一种化合价 |
考点:元素周期律和元素周期表的综合应用
专题:元素周期律与元素周期表专题
分析:由元素在周期表中的位置,可知a为He、b为O、c为F、d为Si、e为P、f为Br.
A.同周期自左而右,原子半径减小,同主族自上而下原子半径增大;
B.硅单质形成原子晶体,其它元素单质形成分子晶体;
C.HF分子之间存在氢键,沸点高于HBr;
D.氧元素化合价有0、-1、-2价.
A.同周期自左而右,原子半径减小,同主族自上而下原子半径增大;
B.硅单质形成原子晶体,其它元素单质形成分子晶体;
C.HF分子之间存在氢键,沸点高于HBr;
D.氧元素化合价有0、-1、-2价.
解答:
解:由元素在周期表中的位置,可知a为He、b为O、c为F、d为Si、e为P、f为Br.
A.同周期自左而右,原子半径减小,同主族自上而下原子半径增大,故原子半径:e>b>c,故A错误;
B.硅单质形成原子晶体,其它元素单质形成分子晶体,硅单质熔点、沸点最高,故B正确;
C.HF分子之间存在氢键,沸点高于HBr,故C错误;
D.氧元素化合价有0、-1、-2价,故D错误,
故选B.
A.同周期自左而右,原子半径减小,同主族自上而下原子半径增大,故原子半径:e>b>c,故A错误;
B.硅单质形成原子晶体,其它元素单质形成分子晶体,硅单质熔点、沸点最高,故B正确;
C.HF分子之间存在氢键,沸点高于HBr,故C错误;
D.氧元素化合价有0、-1、-2价,故D错误,
故选B.
点评:本题考查结构性质位置关系应用,难度不大,注意整体把握元素周期表的结构,掌握氢键对物质性质的影响.

练习册系列答案
相关题目
下列物质存在顺反异构的是( )
| A、1-丁烯 |
| B、2-氯丙烯 |
| C、2-甲基-2-丁烯 |
| D、2─丁烯 |
一溴代烃A经水解后再氧化得到有机物B,A 的一种同分异构体经水解得到有机物C,B和C可发生酯化反应生成酯D,则D 可能是( )
| A、(CH3)2CHCOOCH (CH3)2 |
| B、(CH3)2CHCOOCH(CH3)CH2CH3 |
| C、(CH3)2CHCOOCH2CH(CH3)2 |
| D、CH3(CH2)2COOCH2(CH2)2CH3 |
下列说法中正确的是( )
| A、25℃时,向CH3COONa溶液中加入适量CH3COOH使混合液pH=7,此时溶液中C(Na+)=C(CH3COO-) |
| B、25℃时,0.1 mol?L-1氨水和0.05mol?L-氨水中OH-浓度之比是2:1 |
| C、体积相同、pH值相同的①盐酸 ②硫酸 ③醋酸,被NaOH溶液完全中和,消耗NaOH溶液体积由小到大的顺序是②<①<③ |
| D、向含有HCO3-、CH3COO-、CO32-、SO32-离子的溶液中加入足量的Na2O2固体后,假设溶液体积不变,则以上四种离子浓度基本保持不变的是CO32-和CH3COO- |
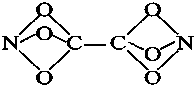 某学生利用C、N、O三种原子拼接成了一种新型分子TetranitiBtoxycarbon(结构如图所示),科学家经过研究发现,这种分子具有良好的贮能特性,一旦被合成完全可用于制造新的炸药.下列有关说法正确的是( )
某学生利用C、N、O三种原子拼接成了一种新型分子TetranitiBtoxycarbon(结构如图所示),科学家经过研究发现,这种分子具有良好的贮能特性,一旦被合成完全可用于制造新的炸药.下列有关说法正确的是( )| A、该分子的分子式为CNO3 |
| B、分子中既含极性键又含非极性键 |
| C、C、N的化合价分别为+4、+3 |
| D、该物质为高分子化合物 |
下列化学(或离子)方程式正确的是( )
| A、乙酸与碳酸钠溶液反应:2H++CO32-═CO2↑+H2O | |||
B、C6H6+HNO3
| |||
| C、亚硫酸的电离方程式:H2SO3?2H++SO32- | |||
| D、醋酸溶液与新制氢氧化铜反应:CH3COOH+OH-→CH3COO-+H2O |
下列有关有机化学实验的说法中,错误的是( )
| A、除去乙醇中少量乙酸:加入足量生石灰蒸馏 |
| B、乙烯和乙醇都能使酸性KMnO4溶液褪色 |
| C、实验室里制备少量乙酸乙酯可用饱和Na2CO3溶液接收生成物 |
| D、分离甘油和氯化钠溶液用分液的方法 |
结合图判断,下列叙述正确的是( )


| A、Ⅰ和Ⅱ中正极均被保护 |
| B、Ⅰ和Ⅱ中负极反应均是:Fe-2e-═Fe2+ |
| C、Ⅰ正极反应是:O2+2H2O+4e-═4OH- |
| D、Ⅰ和Ⅱ中分别加入少量KSCN溶液,溶液均变红 |
 X、Y、Z均为短周期元素,它们在周期表中相对位置如图所示.若Y原子的最外层电子是次外层电子数的3倍,下列说法正确的是( )
X、Y、Z均为短周期元素,它们在周期表中相对位置如图所示.若Y原子的最外层电子是次外层电子数的3倍,下列说法正确的是( )| A、原子半径:X<Z<W |
| B、非金属性:Y>Z |
| C、最高化合价:X<Y |
| D、最高价氧化物对应水化物的酸性:W>Z |