题目内容
15.下列溶液中有关微粒的物质的量浓度关系正确的是( )| A. | 1mol•L-1的(NH4)2Fe(SO4)2•6H2O溶液中:c(NH4+)=c(SO42-)>c(Fe2+)>c(H+) | |
| B. | 等pH的①(NH4)2SO4溶液 ②NH4HSO4溶液 ③NH4Cl溶液中,c(NH4+)的大小关系:①>③>② | |
| C. | 0.1 mol•L-1的NaHCO3溶液:c(Na+)>c(OH-)>c(HCO3-)>c(H+) | |
| D. | 标准状况下将2.24L CO2气体通入150mL 1mol•L-1的NaOH溶液中,充分反应后溶液中c(HCO3-)>c(CO32-) |
分析 A.铵根离子和亚铁离子相互抑制水解且水解但程度较小,硫酸根离子不水解,溶液呈酸性,再结合物料守恒判断;
B.等pH的①(NH4)2SO4溶液 ②NH4HSO4溶液 ③NH4Cl溶液中,铵根离子水解程度越大该溶液浓度越小;
C.碳酸氢钠中碳酸氢根离子水解程度大于电离程度,溶液呈碱性,且其电离和水解程度都较小;
D.标况下2.24L二氧化碳的物质的量是0.1mol,n(NaOH)=1mol/L×0.15L=0.15mol,令溶液中Na2CO3、NaHCO3的物质的量分别为xmol、ymol,根据钠离子、碳原子守恒列方程计算x、y的值,再判断CO32-和HCO3-的物质的量浓度.
解答 解:A.铵根离子和亚铁离子相互抑制水解且水解但程度较小,硫酸根离子不水解,溶液呈酸性,再结合物料守恒得c(SO42-)>c(NH4+)>c(Fe2+)>c(H+),故A错误;
B.等pH的①(NH4)2SO4溶液 ②NH4HSO4溶液 ③NH4Cl溶液中,铵根离子水解程度越大该溶液浓度越小,氢离子抑制铵根离子水解,硫酸铵和氯化铵中铵根离子水解程度相同但硫酸铵中铵根离子个数多,所以c(NH4+)的大小关系:①<②<③,故B错误;
C.碳酸氢钠中碳酸氢根离子水解程度大于电离程度,溶液呈碱性,且其电离和水解程度都较小,所以离子浓度大小顺序是c(Na+)>c(HCO3-)>c(OH-)>c(H+),故C错误;
D.标况下2.24L二氧化碳的物质的量是0.1mol,n(NaOH)=1mol/L×0.15L=0.15mol,令溶液中Na2CO3、NaHCO3的物质的量分别为xmol、ymol,
根据钠离子、碳原子守恒列方程,则:
2x+y=0.15
x+y=0.1,
解得:x=0.05,y=0.05,
即溶质为等浓度的碳酸钠和碳酸氢钠,碳酸钠的水解程度比碳酸氢钠的大,碳酸钠水解生成碳酸氢钠,故c(HCO3-)>c(CO32-),故D正确;
故选D.
点评 本题考查离子浓度大小比较,为高频考点,涉及弱电解质的电离和盐类水解,明确溶液中溶质及其性质是解本题关键,难点是D选项,题目难度中等.

 同步轻松练习系列答案
同步轻松练习系列答案 课课通课程标准思维方法与能力训练系列答案
课课通课程标准思维方法与能力训练系列答案| 化学键 | H-H | O=O |
| 键能/kJ/mol | 436 | 498 |
| A. | 463.4kJ/mol | B. | 926.8kJ/mol | C. | 221.6kJ/mol | D. | 413kJ/mol |
| A. | 含1.2NA个离子的固体Na2O2溶于水配成1L溶液,所得溶液中Na+的物质的量浓度为0.6mol•L-1 | |
| B. | Na在空气中长期放置变成Na2CO3粉末 | |
| C. | 过量的澄清石灰水分别与Na2CO3溶液和NaHCO3溶液反应,现象不同 | |
| D. | 滴加KSCN显红色的溶液中可大量存在NH4+、K+、Cl-、I- |

下列叙述不正确的是( )
| A. | X、Y和Z均能使溴水褪色 | |
| B. | Y既能发生取代反应,也能发生加成反应 | |
| C. | X和Z均能与NaHCO3溶液反应放出CO2 | |
| D. | Y可作加聚反应单体,X可作缩聚反应单体 |
| A. | 常温常压下,16g O2和32g O3的混合物中,含有O原子数月为3NA | |
| B. | 标准状况下,1mol Na2O和1mol Na2O2的混合物中,含有离子总数为7NA | |
| C. | 1 mol NaBH4中离子键的数目为2NA | |
| D. | 在K${\;}_{\;}^{35}$ClO3+6H${\;}_{\;}^{37}$Cl═KCl+3Cl2↑+3H2O中,若生成71 g Cl2,转移的电子数目为$\frac{5}{3}$NA |
| A. | 0.1mol•L-1的(NH4)2SO4溶液中:c(SO42-)>c(NH4+)>c(H+)>c(OH-) | |
| B. | 0.1mol•L-1的NaHCO3溶液中:c(Na+)=c(HCO3-)+c(H2CO3)+2c(CO32-) | |
| C. | 0.1mol•L-1的氨水中:c(H+)=c(OH-) | |
| D. | 在25℃100mL NH4Cl溶液中:c(Cl-)=c(NH4+)+c(NH3•H2O) |
 .
. $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$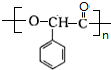 +nH2O.
+nH2O.