题目内容
靛玉红是一种暗红色针状结晶,具有抗菌消炎抗肿瘤等作用,某校合作学习小组的同学拟测定其组成,已知靛玉红由C、H、O、N四种元素组成,相对分子质量为147,实验流程如下: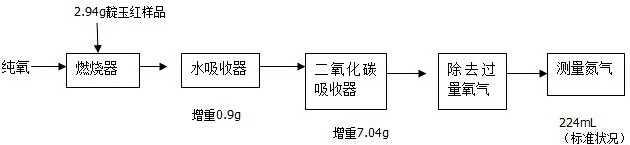
假定在燃烧器中C、H、N分别完全转化为CO2、H2O、N2.请回答下列问题:
(1)靛玉红样品的物质的量为 ;
(2)生成的氮气的物质的量为 ;
(3)靛玉红中碳元素的质量分数为 ;
(4)2.94g靛玉红样品中氧元素的质量为 g;
(5)靛玉红的分子式为 .

假定在燃烧器中C、H、N分别完全转化为CO2、H2O、N2.请回答下列问题:
(1)靛玉红样品的物质的量为
(2)生成的氮气的物质的量为
(3)靛玉红中碳元素的质量分数为
(4)2.94g靛玉红样品中氧元素的质量为
(5)靛玉红的分子式为
考点:有机物实验式和分子式的确定,有关有机物分子式确定的计算
专题:有机化学基础
分析:(1)根据n=
计算靛玉红的物质的量;
(2)根据n=
计算氮气的物质的量;
(3)根据二氧化碳的质量计算二氧化碳的物质的量,根据C守恒计算靛玉红中碳的质量分数;
(4)根据水的质量计算靛玉红中氢的质量,用总质量减去碳、氢、氮的质量即得氧的质量,进而计算氧元素的质量分数;
(5)计算出碳、氢、氧、氮原子个数比,写出实验式,根据相对分子质量确定靛玉红的分子式.
| m |
| M |
(2)根据n=
| V |
| Vm |
(3)根据二氧化碳的质量计算二氧化碳的物质的量,根据C守恒计算靛玉红中碳的质量分数;
(4)根据水的质量计算靛玉红中氢的质量,用总质量减去碳、氢、氮的质量即得氧的质量,进而计算氧元素的质量分数;
(5)计算出碳、氢、氧、氮原子个数比,写出实验式,根据相对分子质量确定靛玉红的分子式.
解答:
解:(1)靛玉红的物质的量为:
=0.02mol,故答案为:0.02mol;
(2)氮气物质的量=
=0.01mol,故答案为:0.01mol;
(3)二氧化碳的物质的量为:
=0.16mol,碳的质量分数=
×100%=7.04X12÷(44X2.94)=65.31%,故答案为:65.3%;
(4)水的物质的量为:
=0.05mol,含氢0.1mol,氧元素质量=2.94g-(0.16mol×12g/mol)-0.1mol×1g/mol-0.01mol×28g/mol=0.64g,
故答案为:0.64;
(5)碳、氢、氧、氮原子个数比=0.16mol:0.1mol:
:0.02mol=8:5:2:1,即最简式为:C8H5O2N,式量为:12×8+5+16×2+14=147,和靛玉红相对分子质量相等,故靛玉红的分子式为:C8H5O2N,故答案为:C8H5O2N.
| 2.94g |
| 147g/mol |
(2)氮气物质的量=
| 0.224L |
| 22.4L/mol |
(3)二氧化碳的物质的量为:
| 7.04g |
| 44g/mol |
| 0.16mol×12g/mol |
| 2.94g |
(4)水的物质的量为:
| 0.9g |
| 18g/mol |
故答案为:0.64;
(5)碳、氢、氧、氮原子个数比=0.16mol:0.1mol:
| 0.64g |
| 16g/mol |
点评:本题考查了有机物实验式和分子式的确定,要根据燃烧产物计算元素的含量,注意质量守恒定律的应用.

练习册系列答案
相关题目
下列关于稀有气体的叙述不正确的是( )
| A、各原子轨道电子均已填满 |
| B、其原子与同周期ⅠA、ⅡA族阳离子具有相同的核外电子排布 |
| C、化学性质非常不活泼 |
| D、同周期中第一电离能最大 |
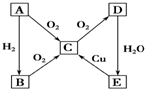 在通常状况下,A为固态单质.根据图转化关系,回答:
在通常状况下,A为固态单质.根据图转化关系,回答: