题目内容
5.下列叙述正确的是( )| A. | SiO2是酸性氧化物,不能与任何酸溶液反应 | |
| B. | 常温下浓硫酸能使铝发生钝化,可在常温下用铝制容器贮运浓硫酸 | |
| C. | 测定中和反应的反应热时,将碱缓慢倒入酸中,所测温度值偏大 | |
| D. | 新制氯水显酸性,向其中滴加少量紫色石蕊试液,充分振荡后溶液呈红色 |
分析 A.二氧化硅能够与氢氟酸反应;
B.浓硫酸具有强的氧化性,能够使铝钝化;
C.测定中和反应的反应热时,将碱缓慢倒入酸中,导致热量损失过大;
D.新制氯水含有HClO,具有漂白性.
解答 解:A.二氧化硅能够与氢氟酸反应生成四氟化硅和水,故A错误;
B.浓硫酸具有强的氧化性,能够使铝钝化,阻止反应的进行,所以可在常温下用铝制容器贮运浓硫酸,故B正确;
C.测定中和反应的反应热时,将碱缓慢倒入酸中,导致热量损失过大,所测温度值偏小,故C错误;
D.新制氯水含有HClO,具有漂白性,向其中滴加少量紫色石蕊试液,溶液先变红后褪色,故D错误;
故选:B.
点评 本题考查元素化合物的知识,涉及二氧化硅、NH3、浓硫酸、氯水等物质的性质,题目难度中等,本题注意把握相关物质的性质,注重相关基础知识的积累.

练习册系列答案
相关题目
15.下列叙述正确的是( )
| A. | 1.00mol NaCl中含有6.02×1023个NaCl分子 | |
| B. | 1.00mol NaCl中,所有Na+的最外层电子总数为8×6.02×1023 | |
| C. | 欲配置1.00L,1.00mol.L-1的NaCl溶液,可将58.5g NaCl溶于1.00L水中 | |
| D. | 电解58.5g 熔融的NaCl,能产生22.4L氯气(标准状况)、23.0g金属钠 |
16.用NA表示阿伏加德罗常数的值,下列叙述中正确的是( )
| A. | 分别用H2O2、KMnO4分解制O2,当制得等质量O2时,转移电子数之比为1:1 | |
| B. | 常温下,0.1 mol•L-1 NH4NO3溶液中含有的氮原子数是0.2NA | |
| C. | 常温常压下,3.2 g O2和3.2 g O3所含氧原子数都是0.2NA | |
| D. | 1mol 甲基所含电子数约为10NA |
13.设NA 为阿伏加德罗常数的值.下列说法正确的是( )
| A. | 3.4gNH3中含N-H键数目为0.2NA | |
| B. | 标准状况下,体积相同的两种气体的分子数一定相同 | |
| C. | 标准状况下,22.4L甲醇中含有的氧原子数目为1.0NA | |
| D. | 1L0.1mol•L-1的Fe2(SO4)3溶液中,Fe3+的数目为0.2NA |
20.如图装置中(烧杯中均盛有海水),铁不易被腐蚀的是( )
| A. |  | B. | 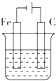 | C. |  | D. |  |
14.下列说法错误的是( )
| A. | 青霉素有青霉素F、G、X、K、V | |
| B. | 因碘酒使蛋白质变性,故常用于外用消毒 | |
| C. | 在奶粉中添加三聚氰胺来提高蛋白质的含量 | |
| D. | 氨基酸是至少含有一个氨基和一个羧基的化合物 |


 .
. 、
、 .
.