题目内容
15.下列装置中,将电能转化为化学能的是( ) | 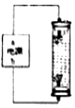 |  |  |
| A.火力发电 | B.用食盐水自制消毒液 | C.用手机打电话 | D.硅太阳能电池 |
| A. | A | B. | B | C. | C | D. | D |
分析 将电能转化为化学能能,应为电解池装置,结合能量的转化特点判断,然后选择即可.
解答 解:A.火力发电是将化学能最终转化为内能,将内能转化为机械能,最后将机械能转化为电能的过程,故A错误;
B.用食盐水自制消毒液为电解装置,是电能转化为化学能的装置,故B正确;
C.用手机打电话,锂电池处于放电状态,故消耗电池内部的化学能,产生电能,故是将化学能转化为电能的过程,故C错误;
D.硅太阳能电池是光能转化为电能的装置,为原电池,故D错误.
故选:B.
点评 本题考查原电池和电解池知识,侧重于学生的分析能力和电化学知识的综合考查,为高考常见题型和高频考点,注意把握常见能量的转化形成,难度不大.

练习册系列答案
相关题目
4.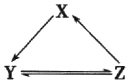 下表所列各组物质中,物质之间通过一步反应不能实砚如图所示转化的是( )
下表所列各组物质中,物质之间通过一步反应不能实砚如图所示转化的是( )
 下表所列各组物质中,物质之间通过一步反应不能实砚如图所示转化的是( )
下表所列各组物质中,物质之间通过一步反应不能实砚如图所示转化的是( )| 选项 | X | Y | Z |
| A | Na | NaOH | NaCl |
| B | Si | SiO2 | Na2SiO3 |
| C | Cl2 | HClO | NaClO |
| D | NO | NO2 | HNO3 |
| A. | A | B. | B | C. | C | D. | D |
6.a g 下列物质在氧气中充分燃烧后的气体(1.01×105 Pa,120℃),通过足量的过氧化钠充分反应后,过氧化钠增重b g,符合b>a的选项有( )
| A. | HCHO | B. | CH3COOCH2CH3 | C. | HOOCCOOH | D. | HCOOH |
3.食醋(主要成分CH3COOH)、纯碱(Na2CO3)和小苏打(NaHCO3)均为家庭厨房中常用的物质.己知:
请回答下列问题:
(1)25℃时,0.10mol•L-1Na2CO3溶液的pH=11,则溶液中由水电离出的c(OH-)=10-3
(2)常温下,将20mL0.10mol•L-1CH3COOH溶液和 20mL0.10mol•L-1HNO2 溶液分别与 20mL 0.10mol•L-1NaHCO3溶液混合(混合后溶液体积变化忽略不计).
①反应开始时,v (CH3COOH )<v (HNO2)(填“>”、“<”或“:”).
②充分反应后.两溶液中c(CH3COO-)< c(NO2-)(填“>”、“<”或“=”).
(3)25℃时,向CH3COOH溶液中加入一定量的NaHCO3,所得混合液的pH=6,则混合液中$\frac{c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)}$=18;
(4)常温下,下列方法可以使0.1mol•L-1CH3COOH的电离程度增大的是bc.
a.加入少量的稀盐酸
b.加热溶液
c.加水稀释
d.加入少量冰醋酸.
| 弱酸 | CH3COOH | H2CO3 | HNO2 |
| 电离常数 | K=1.8×10-5 | K=4.3×10-7 K=5.6×10-11 | K=5.0×10-4 |
(1)25℃时,0.10mol•L-1Na2CO3溶液的pH=11,则溶液中由水电离出的c(OH-)=10-3
(2)常温下,将20mL0.10mol•L-1CH3COOH溶液和 20mL0.10mol•L-1HNO2 溶液分别与 20mL 0.10mol•L-1NaHCO3溶液混合(混合后溶液体积变化忽略不计).
①反应开始时,v (CH3COOH )<v (HNO2)(填“>”、“<”或“:”).
②充分反应后.两溶液中c(CH3COO-)< c(NO2-)(填“>”、“<”或“=”).
(3)25℃时,向CH3COOH溶液中加入一定量的NaHCO3,所得混合液的pH=6,则混合液中$\frac{c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)}$=18;
(4)常温下,下列方法可以使0.1mol•L-1CH3COOH的电离程度增大的是bc.
a.加入少量的稀盐酸
b.加热溶液
c.加水稀释
d.加入少量冰醋酸.
10.25℃时,将浓度均为0.1mol/L、体积分别为Va 和Vb 的HA溶液与BOH溶液按不同体积比混合,保持Va+Vb=100mL,Va、Vb与混合液的pH的关系如图所示. 下列说法正确的是( )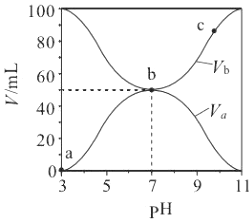

| A. | Ka(HA)的值与 Kb(BOH) 的值不相等 | |
| B. | b 点时,水电离出的 c(H+)=10-7mol/L | |
| C. | c 点时,c(A-)>c(B+) | |
| D. | a→c 过程中$\frac{c({A}^{-})}{c(O{H}^{-})•c(HA)}$不变 |
20.下列生活中常见用品与其类别或主要成分对应不正确的是( )
| A | B | C | D | |
| 用品名称 |  太阳能电池 |  食用油 |  84消毒液 |  合成纤维宇航服 |
| 类别或 主要成分 | SiO2 | 酯类物质 | 混合物 | 高分子材料 |
| A. | A | B. | B | C. | C | D. | D |
7.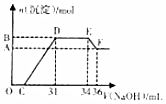 硝酸越稀还原产物中氮元素的化合价越低.某同学取铁铝合金与足量很稀的硝酸充分反应没有气体放出.在反应后的溶液中逐渐加入4mol•L-1NaOH溶液,所加NaOH溶液的体积与产生的沉淀的物质的量的关系如图所示(不考虑沉淀的微量溶解).下列说法正确的是( )
硝酸越稀还原产物中氮元素的化合价越低.某同学取铁铝合金与足量很稀的硝酸充分反应没有气体放出.在反应后的溶液中逐渐加入4mol•L-1NaOH溶液,所加NaOH溶液的体积与产生的沉淀的物质的量的关系如图所示(不考虑沉淀的微量溶解).下列说法正确的是( )
 硝酸越稀还原产物中氮元素的化合价越低.某同学取铁铝合金与足量很稀的硝酸充分反应没有气体放出.在反应后的溶液中逐渐加入4mol•L-1NaOH溶液,所加NaOH溶液的体积与产生的沉淀的物质的量的关系如图所示(不考虑沉淀的微量溶解).下列说法正确的是( )
硝酸越稀还原产物中氮元素的化合价越低.某同学取铁铝合金与足量很稀的硝酸充分反应没有气体放出.在反应后的溶液中逐渐加入4mol•L-1NaOH溶液,所加NaOH溶液的体积与产生的沉淀的物质的量的关系如图所示(不考虑沉淀的微量溶解).下列说法正确的是( )| A. | D点溶液中存在:c(NH4+)+c(Na+)+c(H+)═c(OH-)+c(NO3-) | |
| B. | EF段发生反应的离子方程式为:Al(OH)3+OH-═AlO2-+2H2O | |
| C. | D点溶液中n(NH4+)=0.012mol | |
| D. | 由水电离产生的c(H+):O点>F点 |
4.设NA为阿伏伽德罗常数的值.下列说法正确的是( )
| A. | 100 mL 0.2 mol•L-1蔗糖溶液中所含分子总数为0.02NA | |
| B. | 40mL 10mol•L-1的浓盐酸与足量的MnO2充分反应,生成氯气的分子数为0.1NA | |
| C. | 标准状况下,22.4L CHCl3中含有的氯原子数目为3NA | |
| D. | 14g CO 和N2混合气体中含有的电子总数为7NA |
5.氮化硅(Si3N4)是一种新型的耐高温耐磨材料,氮化硅属于( )
| A. | 离子晶体 | B. | 分子晶体 | C. | 金属晶体 | D. | 原子晶体 |