题目内容
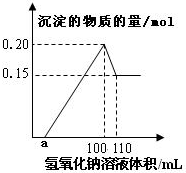 某实验小组对一含有Al3+的未知溶液进行分析,经定量分析后,给出沉淀的物质的量与滴入氢氧化钠体积的关系图:则下列说法中错误的是( )
某实验小组对一含有Al3+的未知溶液进行分析,经定量分析后,给出沉淀的物质的量与滴入氢氧化钠体积的关系图:则下列说法中错误的是( )| A、该未知溶液中至少含有3种阳离子 |
| B、滴加的NaOH溶液的物质的量浓度为5mol/L |
| C、若另一种离子为二价阳离子,则a=10 |
| D、若将最终沉淀过滤、洗涤、灼烧,其质量一定为6g |
考点:有关混合物反应的计算
专题:
分析:A、依据实验过程分析滴入氢氧化钠无沉淀,说明含有H+,继续滴入氢氧化钠溶液生成白色沉淀说明一定生成氢氧化铝沉淀,说明溶液中含有Al3+,加入过量的氢氧化钠溶液沉淀减少,但未完全消失,图象分析说明溶液中除了铝离子,应还有另一种金属阳离子;
B、依据图象分析溶解的氢氧化铝物质的量为0.20mol-0.15mol=0.05mol,消耗氢氧化钠溶液体积=110ml-100ml=10ml,氢氧化钠的浓度=
=5mol/L;
C、若另一种阳离子为二价金属阳离子,依据离子反应过程金属分析判断,氢氧化铝形成最大沉淀量0.05mol,二价金属物质的量为0.15mol,消耗氢氧化钠物质的量为0.05mol×3+0.15mol×2+a×10-3L×5mol/L=0.1L×5mol/L,a=10ml;
D、最后得到的沉淀不能确定其成分,所以不能计算灼烧后得到的氧化物的质量.
B、依据图象分析溶解的氢氧化铝物质的量为0.20mol-0.15mol=0.05mol,消耗氢氧化钠溶液体积=110ml-100ml=10ml,氢氧化钠的浓度=
| 0.05mol |
| 0.01L |
C、若另一种阳离子为二价金属阳离子,依据离子反应过程金属分析判断,氢氧化铝形成最大沉淀量0.05mol,二价金属物质的量为0.15mol,消耗氢氧化钠物质的量为0.05mol×3+0.15mol×2+a×10-3L×5mol/L=0.1L×5mol/L,a=10ml;
D、最后得到的沉淀不能确定其成分,所以不能计算灼烧后得到的氧化物的质量.
解答:
解:A、实验过程分析滴入氢氧化钠无沉淀,说明含有H+,继续滴入氢氧化钠溶液生成白色沉淀说明一定生成氢氧化铝沉淀,说明溶液中含有Al3+,加入过量的氢氧化钠溶液沉淀减少,图象分析说明溶液中除了铝离子,应还有另一种金属阳离子,该未知溶液中至少含有3种阳离子,故A正确;
B、依据图象分析溶解的氢氧化铝物质的量为0.20mol-0.15mol=0.05mol,消耗氢氧化钠溶液体积=110ml-100ml=10ml,氢氧化钠的浓度=
=5mol/L,故B正确;
C、若另一种阳离子为二价金属阳离子,生成氢氧化铝最大沉淀量0.05mol,二价金属物质的量为0.15mol,开始消耗氢氧化钠体积为aml,消耗氢氧化钠物质的量为0.05mol×3+0.15mol×2+a×10-3L×5mol/L=0.1L×5mol/L,a=10,故C正确;
D、最后得到的沉淀不能确定其成分,所以不能计算灼烧后得到的氧化物的质量,故D错误;
故选D.
B、依据图象分析溶解的氢氧化铝物质的量为0.20mol-0.15mol=0.05mol,消耗氢氧化钠溶液体积=110ml-100ml=10ml,氢氧化钠的浓度=
| 0.05mol |
| 0.01L |
C、若另一种阳离子为二价金属阳离子,生成氢氧化铝最大沉淀量0.05mol,二价金属物质的量为0.15mol,开始消耗氢氧化钠体积为aml,消耗氢氧化钠物质的量为0.05mol×3+0.15mol×2+a×10-3L×5mol/L=0.1L×5mol/L,a=10,故C正确;
D、最后得到的沉淀不能确定其成分,所以不能计算灼烧后得到的氧化物的质量,故D错误;
故选D.
点评:本题考查了图象分析的方法掌握,物质性质的分析应用,定量计算和图象中的定量分析是解题关键,题目难度较大.

练习册系列答案
相关题目
下列化学用语或模型表示正确的是( )
A、硝基苯的结构简式: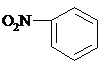 |
B、COCl2分子的电子式: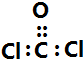 |
C、过氧化氢的电子式: |
D、NaCl的晶体模型: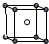 |
下列水溶液中的各组离子能大量共存的是( )
| A、Na+、Ba2+、Cl-、SO42- |
| B、Ca2+、NO3-、C1-、K+ |
| C、Cu2+、K+、OH-、Cl- |
| D、H+、Cl-、Na+、CO32- |
下列表示对应化学反应的离子方程式正确的是( )
| A、AlCl3溶液中加入过量的浓氨水:Al3++4NH3?H2O=[Al(OH)4]-+4NH4+ |
| B、用FeCl3溶液腐蚀铜线路板:Cu+2Fe3+=Cu2++2Fe2+ |
| C、大理石溶于醋酸中的反应:CaCO3+2H+=Ca2++H2O+CO2↑ |
| D、钠与水反应:Na+2H2O=Na++2OH-+H2↑ |
下列反应的离子方程式不正确的是( )
| A、铁与氯化铁溶液:2Fe3++Fe═3Fe2+ |
| B、氯气与溴化钠溶液:2Br-+Cl2═Br2+2Cl- |
| C、硫酸铵和氢氧化钡溶液:Ba2++SO42-═BaSO4↓ |
| D、铜与稀硝酸:3Cu+8H++2NO3-═Cu2++2NO↑+4H2O |
下列有关实验操作的说法错误的是( )
| A、中和滴定时盛待测液的锥形瓶中有少量水对滴定结果无影响 |
| B、在酸碱中和滴定实验中,滴定管都需润洗,否则引起误差 |
| C、滴定时,左手控制滴定管活塞,右手握持锥形瓶,边滴边振荡,眼睛注视滴定管中的液面 |
| D、称量时,称量物放在称量纸上,置于托盘天平的左盘,砝码放在托盘天平的右盘 |
设NA为阿伏伽德罗常数的值,下列说法中正确的是( )
| A、常温常压下,4.6g NO2含有0.2NA个氧原子 |
| B、0.1mol Na2O2固体中含有离子总数为0.4NA |
| C、标准状况下2.24L Cl2与足量的铁充分反应,转移电子数为0.3NA |
| D、等物质的量的NO和CO2所含分子数均为NA |
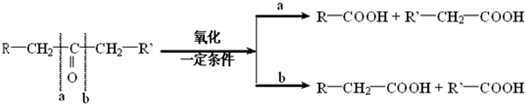

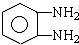 )缩聚生成一种合成纤维:
)缩聚生成一种合成纤维: