题目内容
实验室可用氯气与金属铁反应制备无水三氯化铁,该化合物呈棕红色。易潮解,100℃左右时升华。图是两个学生设计的实验装置,左边的反应装置相同,而右边的产品收集装置则不同,分别如(Ⅰ)和(Ⅱ)所示。试回答:
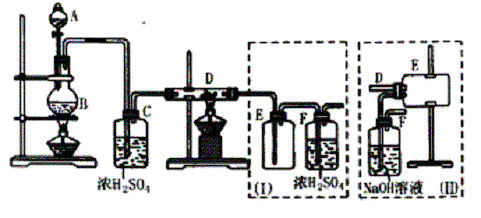
⑴B中反应的化学方程式为 。
⑵D中的反应开始前,需排除装置中的空气,应采取的方法是 。
⑶D中反应的化学方程式为 。
⑷装置(Ⅰ)的主要缺点是 。
⑸装置(Ⅱ)的主要缺点是 。如果选取用此装置来完在实验,则必须采取的改进措施是 。
答案:
解析:
提示:
解析:
⑴MnO2+4HCl(浓) ⑵在B中的反应进行一段时间后,看到黄绿色气体充满装置,再开始加热D ⑶2Fe+3Cl2==2FeCl3 ⑷导管易被产品堵塞;尾气排入空气,造成污染 ⑸产品易潮解; 在E、F瓶这间连接装有干燥剂的装置
|
提示:
由题意“制备FeCl3”可知D管中应是铁粉,A、B装置是Cl2发生装置,C装置是干燥Cl2装置,要使D管中的空气排出,最方便的方法是让产生的Cl2驱赶空气,因此D处先不要加热,待D管中充满Cl2后再加热,以保证Cl2与Fe反应生成FeCl3无杂质。由于氯化铁易升华,因此在D管中的FeCl3易挥发出,而装置I中导气管太细,FeCl3易冷凝而在此堵塞,并且多余的Cl2不能被浓H2SO4吸收,排出的尾气会污染空气。在装置Ⅱ中,由于导气管直接插入NaOH溶液中,会有水汽挥发,导致FeCl3潮解。故应在装置Ⅱ的E、F之间加入一干燥装置。
|

练习册系列答案
 优等生题库系列答案
优等生题库系列答案
相关题目



