题目内容
0.1mol?L-1的下列溶液碱性最强的是( )
| A、CH3COONa |
| B、Na2CO3 |
| C、NaCl |
| D、NaHCO3 |
考点:盐类水解的应用
专题:盐类的水解专题
分析:相同浓度的钠盐溶液,酸根离子水解程度越大,其钠盐溶液pH越大,则盐的碱性越强,据此分析解答.
解答:
解:相同浓度的钠盐溶液,酸根离子水解程度越大,其钠盐溶液pH越大,则盐的碱性越强,NaCl是强酸强碱盐,其溶液呈中性,弱酸根离子水解程度大小顺序是CO32->HCO3->CH3COO-,所以相同浓度的这几种弱酸盐中,碱性强弱书写是Na2CO3>NaHCO3>CH3COONa,所以碱性最强的是Na2CO3,故选B.
点评:本题考查了盐类水解,明确弱酸酸性强弱与酸根离子水解程度的关系是解本题关键,知道常见弱酸的酸性强弱,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
 下列有关右图装置的叙述不正确的是( )
下列有关右图装置的叙述不正确的是( )| A、a和b用导线连接时,铜片上析出金属铜 |
| B、b和a分别连接直流电源正、负极时,SO42-向铁电极移动 |
| C、a和b分别连接直流电源正、负极时,铁片上发生的反应为Cu2++2e-═Cu |
| D、无论a和b怎样连接,铁片均会溶解,溶液从蓝色逐渐变成浅绿色 |
 我国支持“人文奥运”的一个重要体现是:坚决反对运动员服用兴奋剂.某种兴奋剂的结构简式如图所示,有关该物质的说法正确的是( )
我国支持“人文奥运”的一个重要体现是:坚决反对运动员服用兴奋剂.某种兴奋剂的结构简式如图所示,有关该物质的说法正确的是( )| A、该物质遇FeCl3溶液显紫色 |
| B、滴入KMnO4(H+)溶液,观察紫色褪去,能证明结构中存在碳碳双键 |
| C、1 mol该物质与浓溴水和H2反应最多消耗Br2和H2分别为4 mol、7 mol |
| D、该分子中的所有原子有可能共平面 |
下列物质哪些与苯酚互为同系物( )
A、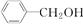 |
B、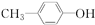 |
C、 |
D、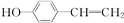 |
如图所示,当向试管内通入21mL O2时,最后试管中的液面仍在原来的位置,则原试管中NO为( )


| A、6mL | B、12mL |
| C、16mL | D、18mL |