题目内容
在所有生物中,硫是构成多种氨基酸的重要元素,其氧化物SO2是形成酸雨的主要成份,而硫酸的产量常用来衡量一个国家发达程度,同时硫的多种化合物在日常生活中作用巨大,所以研究硫及其化合物的性质有重要意义.请回答有关问题:
(1)写出硫元素的原子结构示意图: ;
(2)硫的单质通常以S6和S8两种形式呈出,S6和S8互为 ;
A.同素异形体B.同分异构体C.同系物D.同位素
(3)Cu2S在高温条件下发生如下反应:2Cu2S(s)+3O2(g)═2Cu2O(s)+2SO2(g)△H=-773kJ?mol-1,当该反应生成标准状况下4.48LSO2时,释放出的热量为 kJ;
(4)Na2S溶液在空气中长期放置,和氧气反应生成与过氧化钠的结构及化学性质相似的物质Na2S2,该反应的化学方程式为: ,当生成55gNa2S2时,转移电子的数目为 mol;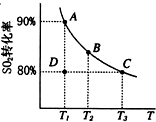
(5)硫酸工业生产中涉及反应:2SO2(g)+O2(g)
2SO3(g).向2L的容器中充入2molSO2、1molO2,SO2的平衡转化率与温度的关系如图所示,请回答:
①T1温度下,反应进行到状态D时,v正 v逆(填“>”、“<”或“=”);
②若在T3温度时,达平衡时测得反应放出的热量为Q1.此时再向容器中加入2molSO2、1molO2并使之重新达到平衡,测得又放出热量Q2.则下列说法正确的是 (填序号字母).
A.容器的压强增大为原来的两倍 B.Q2一定等于Q1
C.重新平衡时SO2的转化率一定大于80% D.T3时的平衡常数大于T1时的平衡常数.
(1)写出硫元素的原子结构示意图:
(2)硫的单质通常以S6和S8两种形式呈出,S6和S8互为
A.同素异形体B.同分异构体C.同系物D.同位素
(3)Cu2S在高温条件下发生如下反应:2Cu2S(s)+3O2(g)═2Cu2O(s)+2SO2(g)△H=-773kJ?mol-1,当该反应生成标准状况下4.48LSO2时,释放出的热量为
(4)Na2S溶液在空气中长期放置,和氧气反应生成与过氧化钠的结构及化学性质相似的物质Na2S2,该反应的化学方程式为:

(5)硫酸工业生产中涉及反应:2SO2(g)+O2(g)
| 催化剂 |
| 高温高压 |
①T1温度下,反应进行到状态D时,v正
②若在T3温度时,达平衡时测得反应放出的热量为Q1.此时再向容器中加入2molSO2、1molO2并使之重新达到平衡,测得又放出热量Q2.则下列说法正确的是
A.容器的压强增大为原来的两倍 B.Q2一定等于Q1
C.重新平衡时SO2的转化率一定大于80% D.T3时的平衡常数大于T1时的平衡常数.
考点:化学平衡的计算,有关反应热的计算,氧化还原反应的计算
专题:
分析:(1)硫原子核外电子数是16,根据原子结构示意图的画法来回答;
(2)S6和S8是硫元素组成的两种物理性质不同的单质;
(3)根据热化学方程式的意义来计算;
(4)Na2S、氧气、水反应生成Na2S2、NaOH,以此书写方程式,由元素的化合价变化计算转移的电子数;
(5)①当反应进行到D状态时,未达到平衡,A点是该温度下的平衡状态,所以二氧化硫的转化率要增大;
②在T3温度时,达平衡时测得反应放出的热量为Q1.此时再向容器中加入2mol SO2、1mol O2,平衡向正反应方向移动,放出的热量增大,等效为增大压强,平衡向正反应方向移动,反应物的转化率增大.平衡常数只与温度有关,由图可知,温度越高SO2的转化率越小,即升高温度平衡向逆反应移动,平衡常数降低.
(2)S6和S8是硫元素组成的两种物理性质不同的单质;
(3)根据热化学方程式的意义来计算;
(4)Na2S、氧气、水反应生成Na2S2、NaOH,以此书写方程式,由元素的化合价变化计算转移的电子数;
(5)①当反应进行到D状态时,未达到平衡,A点是该温度下的平衡状态,所以二氧化硫的转化率要增大;
②在T3温度时,达平衡时测得反应放出的热量为Q1.此时再向容器中加入2mol SO2、1mol O2,平衡向正反应方向移动,放出的热量增大,等效为增大压强,平衡向正反应方向移动,反应物的转化率增大.平衡常数只与温度有关,由图可知,温度越高SO2的转化率越小,即升高温度平衡向逆反应移动,平衡常数降低.
解答:
解:(1)硫原子核外电子数是16,原子结构示意图为: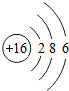 ,故答案为:
,故答案为: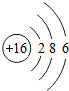 ;
;
(2)S6和S8是硫元素组成的两种物理性质不同的单质,二者互为同素异形体,故选A;
(3)反应2Cu2S(s)+3O2(g)═2Cu2O(s)+2SO2(g)△H=-773kJ?mol-1,表示生成2mol二氧化硫放热773kJ,当该反应生成标准状况下4.48L即0.2molSO2时,释放出的热量为77.3kJ,故答案为:77.3;
(4)Na2S、氧气、水反应生成Na2S2、NaOH,该反应的方程式为4Na2S+O2+2H2O═4NaOH+2Na2S2,S元素的化合价由-2价变为-1价,则当生成55g即0.5mol Na2S2时,转移的电子数为0.5mol×2×(2-1)=1mol,故答案为:4Na2S+O2+2H2O═4NaOH+2Na2S2;1;
(5)①状态D时的SO2的转化率为80%,未达到90%,反应向正反应进行,v正>v逆,故答案为:>;
②在T3温度时,达平衡时测得反应放出的热量为Q1.此时再向容器中加入2mol SO2、1mol O2,平衡向正反应方向移动,放出的热量增大,等效为增大压强,平衡向正反应方向移动,反应物的转化率增大,故容器内压强小于原来的2倍,放出的热量Q2>Q1,故A、B错误,C正确;平衡常数只与温度有关,由图可知,温度越高SO2的转化率越小,即升高温度平衡向逆反应移动,平衡常数降低,故D错误;
故答案为:C.
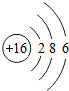 ,故答案为:
,故答案为: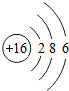 ;
;(2)S6和S8是硫元素组成的两种物理性质不同的单质,二者互为同素异形体,故选A;
(3)反应2Cu2S(s)+3O2(g)═2Cu2O(s)+2SO2(g)△H=-773kJ?mol-1,表示生成2mol二氧化硫放热773kJ,当该反应生成标准状况下4.48L即0.2molSO2时,释放出的热量为77.3kJ,故答案为:77.3;
(4)Na2S、氧气、水反应生成Na2S2、NaOH,该反应的方程式为4Na2S+O2+2H2O═4NaOH+2Na2S2,S元素的化合价由-2价变为-1价,则当生成55g即0.5mol Na2S2时,转移的电子数为0.5mol×2×(2-1)=1mol,故答案为:4Na2S+O2+2H2O═4NaOH+2Na2S2;1;
(5)①状态D时的SO2的转化率为80%,未达到90%,反应向正反应进行,v正>v逆,故答案为:>;
②在T3温度时,达平衡时测得反应放出的热量为Q1.此时再向容器中加入2mol SO2、1mol O2,平衡向正反应方向移动,放出的热量增大,等效为增大压强,平衡向正反应方向移动,反应物的转化率增大,故容器内压强小于原来的2倍,放出的热量Q2>Q1,故A、B错误,C正确;平衡常数只与温度有关,由图可知,温度越高SO2的转化率越小,即升高温度平衡向逆反应移动,平衡常数降低,故D错误;
故答案为:C.
点评:本题考查化学平衡图象与影响因素、化学平衡常数计算、硫化合物的性质、实验方案设计等,题目较为综合,是对知识的综合利用,注意利用等效平衡分析,难度中等.

练习册系列答案
相关题目
已知下列热化学方程式:
Fe2O3(s)+3CO(g)═2Fe(s)+3CO2(g)△H=-24.8kJ?mol-1
Fe2O3(s)+
CO(g)═
Fe3O4(s)+
CO2(g)△H=-15.73kJ?mol-1
Fe3O4(s)+CO(g)═3FeO(s)+CO2(g)△H=+640.4kJ?mol-1
则14g CO气体还原足量FeO固体得到Fe固体和CO2气体时对应的△H约为( )
Fe2O3(s)+3CO(g)═2Fe(s)+3CO2(g)△H=-24.8kJ?mol-1
Fe2O3(s)+
| 1 |
| 3 |
| 2 |
| 3 |
| 1 |
| 3 |
Fe3O4(s)+CO(g)═3FeO(s)+CO2(g)△H=+640.4kJ?mol-1
则14g CO气体还原足量FeO固体得到Fe固体和CO2气体时对应的△H约为( )
| A、-218kJ?mol-1 |
| B、-109kJ?mol-1 |
| C、+218kJ?mol-1 |
| D、+109kJ?mol-1 |
铜片放入热的稀硫酸中无明显现象,当加入下列哪种物质后现象有明显变化的是( )
| A、NaNO3 |
| B、HCl |
| C、NaOH |
| D、KCl |
下列溶液能跟铜片反应,而且铜片的质量会减轻的是( )
| A、盐酸 |
| B、FeCl3溶液 |
| C、AgNO3溶液 |
| D、NaCl溶液 |
若NA表示阿伏加德罗常数的数值,下列叙述中不正确的是( )
| A、16g O2与O3混合物中所含电子数为8NA |
| B、标准状况下,2.24LCH3OH分子中共用电子对数为0.5NA |
| C、6gSiO2晶体中硅氧共价键数为0.4NA |
| D、0.1mol13C18O中所含中子数为1.7NA |
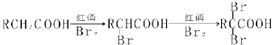
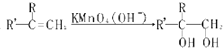

 请用如图的装置设计一个实验,以测定SO2转化为SO3的转化率.
请用如图的装置设计一个实验,以测定SO2转化为SO3的转化率.