题目内容
钛在化合物中的化合价主要有+2、+3、+4。钛铁矿提炼钛目前通常采用“氯化法”,即将钛铁矿与焦炭混合,通入氯气并加热先制得TiCl4,反应为(未配平):
____FeTiO3+____Cl2+_____C![]() ____TiCl4+____FeCl3(s)+ ____CO(g)。再将TiCl4蒸馏出来提纯后,在氩气的保护下与镁共热(1 220 K—1 420 K)制得钛。TiCl4常温下为无色液体(熔点-23.2 ℃,沸点136.4 ℃),易挥发,有刺激性气味,易溶于有机溶剂。下列说法不正确的是( )
____TiCl4+____FeCl3(s)+ ____CO(g)。再将TiCl4蒸馏出来提纯后,在氩气的保护下与镁共热(1 220 K—1 420 K)制得钛。TiCl4常温下为无色液体(熔点-23.2 ℃,沸点136.4 ℃),易挥发,有刺激性气味,易溶于有机溶剂。下列说法不正确的是( )
A.配平后方程式上的系数分别对应为:2 7 6 2 2 6
B.后应中FeTiO3和C是还原剂,Cl2是氧化剂
C.上述反应中每生成2 mol TiCl4,FeTiO3中的Fe失去2 mol电子
D.TiCl4晶体是分子晶体
C
解析:本题反应式学生感到陌生,但经过分析应能得出Cl2是氧化剂,FeTiO3中Fe的化合价为+3,Ti的化合价也为+3,反应中Ti的化合价由+3升高到+4,所以反应中FeTiO3和C是还原剂,所以B项正确;根据得失电子相等,经过配平或验证知A项正确;Fe元素的化合价没变化,所以C项错误;由TiCl4在常温下为无色液体(熔点-23.2 ℃,沸点136.4 ℃),易挥发,有刺激性气味,易溶于有机溶剂,而得知TiCl4晶体为分子晶体。

练习册系列答案
 名牌中学课时作业系列答案
名牌中学课时作业系列答案 明天教育课时特训系列答案
明天教育课时特训系列答案 浙江新课程三维目标测评课时特训系列答案
浙江新课程三维目标测评课时特训系列答案 周周清检测系列答案
周周清检测系列答案
相关题目
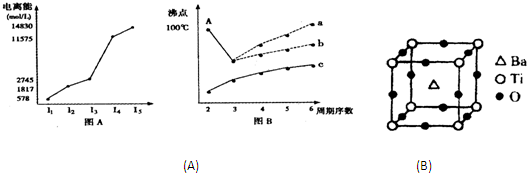
 (1)图表法、图象法是常用的科学研究方法.短周期某主族元素M的电离能情况如图(A)所示.则M元素位于周期表的第
(1)图表法、图象法是常用的科学研究方法.短周期某主族元素M的电离能情况如图(A)所示.则M元素位于周期表的第
 (1) 22Ti元素基态原子价电子的轨道表示式为_______________。
(1) 22Ti元素基态原子价电子的轨道表示式为_______________。