题目内容
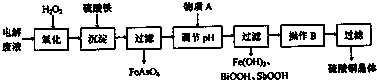
铜电解精炼后的电解液含有多种杂质,工业上常除杂提纯制备硫酸铜.除杂时,溶液中离子的浓度小于1.0×10-5mol?L-1,可认为该离子沉淀完全.Fe(OH)3沉淀时,Sb3+、Bi3+形成SbOOH、BiOOH一起沉淀.某电解液中所含杂质离子如下表,除杂提纯路线如图.
已知:lg2=0.3;Ksp(FeAsO4)=5.7×10-21;Ka=5×10-3
(1)加入H2O2的目的之一是将AsO33-氧化为H3AsO4,其离子方程式是 ;加入H2O2的另外一个目的是 ;
(2)加入足量H2O2后相关物质氧化完全,溶液体积为1.2倍,则加硫酸铁之前有沉淀生成吗?简单计算说明 ;
(3)调节pH值用的物质A为 ;
(4)某温度下,物质A将溶液调节pH为3.3时,Fe3+沉淀完全,该温度下Kw越为1×10-14,则该温度下Fe(OH)3的Ksp约为 ;
(5)操作B为 .
| 离子 | H+ | AsO33- | Sb3+ | Bi3+ | Fe2+ |
| c(mol?L-1) | 1.0 | 3.6×10-3 | 2.4×10-4 | 1.0×10-4 | 2.0×10-3 |

(1)加入H2O2的目的之一是将AsO33-氧化为H3AsO4,其离子方程式是
(2)加入足量H2O2后相关物质氧化完全,溶液体积为1.2倍,则加硫酸铁之前有沉淀生成吗?简单计算说明
(3)调节pH值用的物质A为
(4)某温度下,物质A将溶液调节pH为3.3时,Fe3+沉淀完全,该温度下Kw越为1×10-14,则该温度下Fe(OH)3的Ksp约为
(5)操作B为
考点:物质分离和提纯的方法和基本操作综合应用
专题:
分析:电解液加入双氧水氧化发生的反应为:AsO33-+H2O2+3H+═H3AsO4+H2O;2Fe2++H2O2+2H+═2Fe3++2H2O,再加入硫酸亚铁生成沉淀FeAsO4,过滤除去FeAsO4沉淀,再加入物质A调节PH值使Fe3+、Sb3+、Bi3+形成Fe(OH)3、SbOOH、BiOOH一起沉淀而除去,再蒸发浓缩、冷却结晶、过滤、洗涤、干燥得硫酸铜晶体,
(1)根据以上分析,加入H2O2,其离子方程式AsO33-+H2O2+3H+═H3AsO4+H2O,2Fe2++H2O2+2H+═2Fe3++2H2O根据反应进行分析;
(2)加入足量H2O2后相关物质氧化完全后,溶液体积为1.2倍,则溶液中三价铁离子浓度为:
mol?L-1,AsO43-的浓度为:
=3×10-3mol?L-1,则Qc=
×3×10-3=5×10-6>Ksp(FeAsO4)=5.7×10-21,所以加硫酸铁之前有沉淀生成;
(3)为了不引入新的杂质,则调节pH值用的物质A又能消耗氢离子分析;
(4)Fe(OH)3的Ksp=C(Fe3+)×C(OH-)3进行计算;
(5)根据以上分析,蒸发浓缩、冷却结晶、过滤、洗涤、干燥得硫酸铜晶体;
(1)根据以上分析,加入H2O2,其离子方程式AsO33-+H2O2+3H+═H3AsO4+H2O,2Fe2++H2O2+2H+═2Fe3++2H2O根据反应进行分析;
(2)加入足量H2O2后相关物质氧化完全后,溶液体积为1.2倍,则溶液中三价铁离子浓度为:
| 2.0×10 -3 |
| 1.2 |
| 3.6×10 -3 |
| 1.2 |
| 2.0×10 -3 |
| 1.2 |
(3)为了不引入新的杂质,则调节pH值用的物质A又能消耗氢离子分析;
(4)Fe(OH)3的Ksp=C(Fe3+)×C(OH-)3进行计算;
(5)根据以上分析,蒸发浓缩、冷却结晶、过滤、洗涤、干燥得硫酸铜晶体;
解答:
解:电解液加入双氧水氧化发生的反应为:AsO33-+H2O2+3H+═H3AsO4+H2O;2Fe2++H2O2+2H+═2Fe3++2H2O,再加入硫酸亚铁生成沉淀FeAsO4,过滤除去FeAsO4沉淀,再加入物质A调节PH值使Fe3+、Sb3+、Bi3+形成Fe(OH)3、SbOOH、BiOOH一起沉淀而除去,再蒸发浓缩、冷却结晶、过滤、洗涤、干燥得硫酸铜晶体;
(1)根据以上分析,加入H2O2的目的将AsO33-氧化为H3AsO4,其离子方程式AsO33-+H2O2+3H+═H3AsO4+H2O,加入H2O2的另外一个目的是将二价铁氧化成三价铁;
故答案为:AsO33-+H2O2+3H+═H3AsO4+H2O,将二价铁氧化成三价铁;
(2)加入足量H2O2后相关物质氧化完全后,溶液体积为1.2倍,则溶液中三价铁离子浓度为:
mol?L-1,AsO43-的浓度为:
=3×10-3mol?L-1,则Qc=
×3×10-3=5×10-6>Ksp(FeAsO4)=5.7×10-21,所以加硫酸铁之前有沉淀生成,
故答案为:有;
×3×10-3=5×10-6>Ksp(FeAsO4)=5.7×10-21,有FeAsO4沉淀生成;
(3)为了不引入新的杂质,则调节pH值用的物质A又能消耗氢离子,所以为CuO或者CuCO3,故答案为:CuO或者CuCO3;
(4)Fe(OH)3的Ksp=C(Fe3+)×C(OH-)3=1.0×10-5×(10-10.7)3=10-37.1,故答案为:10-37.1;
(5)根据以上分析,蒸发浓缩、冷却结晶、过滤、洗涤、干燥得硫酸铜晶体,故答案为:蒸发浓缩、冷却结晶;
(1)根据以上分析,加入H2O2的目的将AsO33-氧化为H3AsO4,其离子方程式AsO33-+H2O2+3H+═H3AsO4+H2O,加入H2O2的另外一个目的是将二价铁氧化成三价铁;
故答案为:AsO33-+H2O2+3H+═H3AsO4+H2O,将二价铁氧化成三价铁;
(2)加入足量H2O2后相关物质氧化完全后,溶液体积为1.2倍,则溶液中三价铁离子浓度为:
| 2.0×10 -3 |
| 1.2 |
| 3.6×10 -3 |
| 1.2 |
| 2.0×10 -3 |
| 1.2 |
故答案为:有;
| 2.0×10 -3 |
| 1.2 |
(3)为了不引入新的杂质,则调节pH值用的物质A又能消耗氢离子,所以为CuO或者CuCO3,故答案为:CuO或者CuCO3;
(4)Fe(OH)3的Ksp=C(Fe3+)×C(OH-)3=1.0×10-5×(10-10.7)3=10-37.1,故答案为:10-37.1;
(5)根据以上分析,蒸发浓缩、冷却结晶、过滤、洗涤、干燥得硫酸铜晶体,故答案为:蒸发浓缩、冷却结晶;
点评:考查学生对元素及其化合物的主要性质的掌握、书写离子方程式、阅读题目获取新信息能力、对工艺流程的理解等,难度中等,需要学生具备扎实的基础与综合运用知识、信息分析解决问题能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列物质中,不能电离出酸根离子的是( )
| A、Na2SO3 |
| B、Ba(OH)2 |
| C、KMnO4 |
| D、KCl04 |
等质量的下列物质分别与盐酸反应,消耗HCl的物质的量最少的是( )
| A、Na |
| B、Na2O2 |
| C、Na2CO3 |
| D、Ca(HCO3)2 |
下列各图所示装置的气密性检查中,漏气的是( )
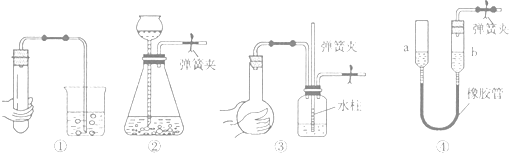

| A、对装置①,双手移去后,导管中水面高于烧杯内水面 |
| B、对装置②,长颈漏斗内液面高度保持不变 |
| C、对装置③,长导管内形成一段水柱 |
| D、对装置④,上下移动a管后,a、b两端液面仍相平 |
 ,
,