题目内容
9.下列各组中的离子,在溶液中能大量共存的是( )| A. | H+ Na+HCO3- Cl- | B. | Cu2+ Na+NO3- SO42- | ||
| C. | Mg2+ H+ SO42-OH- | D. | Ag+ Al3+ Cl-H+ |
分析 离子之间不能结合生成沉淀、气体、水、弱电解质或发生氧化还原反应、络合反应、双水解反应的,则离子能大量共存,据此分析解答.
解答 解:A.H+和HCO3- 反应生成二氧化碳和水而不能大量共存,故A错误;
B.这几种离子之间不反应,所以能大量共存,故B正确;
C.Mg2+、H+分别和OH-反应生成沉淀、弱电解质,所以不能大量共存,故C错误;
D.Ag+和Cl-生成AgCl白色沉淀而不能大量共存,故D错误;
故选B.
点评 本题考查离子共存,为高频考点,明确物质性质及离子共存条件是解本题关键,侧重考查复分解反应,知道常见弱电解质,熟练掌握常见物质溶解性,题目难度不大.

练习册系列答案
 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案
相关题目
14.下列说法正确的是( )
| A. | 强电解质溶液的导电能力一定比弱电解质溶液强 | |
| B. | 中和等体积、等物质的量浓度的盐酸和醋酸溶液,盐酸所需氢氧化钠等于醋酸 | |
| C. | 将氢氧化钠和氨水溶液各稀释一倍,两者的OH-浓度均减少到原来的$\frac{1}{2}$ | |
| D. | 如果盐酸的浓度是醋酸浓度的二倍,则盐酸的H+浓度也是醋酸的二倍 |
20.下列图示与对应的叙述相符的是( )
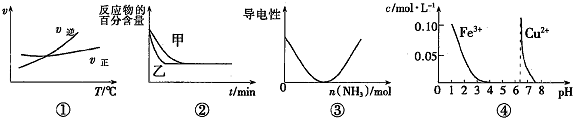

| A. | 据图①可判断可逆反应A2(g)+3B2(g)?2AB3(g)的△H>0 | |
| B. | 图②表示压强对可逆反应2A(g)+B(g)?3C(g)+D(s)的影响,乙的压强大 | |
| C. | 图③可表示乙酸溶液中通入氨气至过量过程中溶液导电性的变化 | |
| D. | 据图④,若除去0.1 mol•L-1CuSO4溶液中混有的Fe3+,可向溶液中加入适量NaOH至pH约为7 |
17.下列变化属于化学变化的是( )
| A. | 过滤除去水中的泥沙 | B. | 食物腐烂 | ||
| C. | 蒸馏法分离酒精与水 | D. | 分液法分离四氯化碳与水 |
4.下列叙述正确的是( )
| A. | 室温时,非金属元素的单质都是气体 | |
| B. | 同一周期中,碱金属的第一电离能最小 | |
| C. | VIA 族元素的原子,其半径越大,越容易得到电子 | |
| D. | 同周期元素中,VIIA 族元素的原子半径最大 |
18.实验报告中,以下数据合理的是( )
| A. | 用碱式滴定管量取25.03mLH2SO4溶液 | |
| B. | 用托盘天平称取11.7gNaCl | |
| C. | 用50mL量筒量取21.48mL稀硫酸 | |
| D. | 用pH试纸测定HNO3溶液的pH=3.7 |
19.下列说法正确的是( )
| A. | SiO2溶于水是酸性 | B. | CO2通入水玻璃可得硅酸 | ||
| C. | SiO2不溶于任何酸 | D. | SiO2晶体中存在单个SiO2分子 |
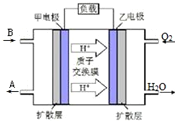 已知A、B、C、D是中学化学常见物质,它们在一定条件下有A+B→C+D的转化关系.
已知A、B、C、D是中学化学常见物质,它们在一定条件下有A+B→C+D的转化关系.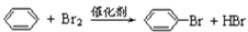 .
.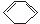 )脱去2mol氢原子变成苯却放热,可推断苯比1,3-环己二烯稳定(填稳定或不稳定).
)脱去2mol氢原子变成苯却放热,可推断苯比1,3-环己二烯稳定(填稳定或不稳定).