题目内容
对于mA(g)+nB(g)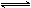 pC(g)+qD(g)的平衡体系,当升高温度时,体系的平均密度对H2的相对密度从16.5变为16.9,则下列说法正确的是
pC(g)+qD(g)的平衡体系,当升高温度时,体系的平均密度对H2的相对密度从16.5变为16.9,则下列说法正确的是
[ ]
Am+n>p+q,正反应是放热反应
B.m+n>p+q,正反应是吸热反应
Cm+n<p+q,逆反应是放热反应
D.m+n<p+q,逆反应是吸热反应
答案:BD
提示:
提示:
|
本题的解题思路可以从混合气平均分子量的变化入手,结合温度变化,推导出平衡移动方向,再推导出反应前后气体体积变化情况,从而得出正确答案.这要经过几次思维的转换才能完成. 题给反应中的反应物和生成物都是气态.原平衡时混合气的平均分子量为 16.5×2=33,升高温度后达新平衡时混合气的平均分子量为16.9×2=33.8.这就说明升高温度达平衡后混合气的平均分子量增大,也就是说升高温度时平衡向气体体积缩小的方向移动,且气体体积缩小的方向是吸热反应的方向.故选项B、D符合题意. |

练习册系列答案
相关题目
|
对于mA(g)+nB(g) | |
A. |
m+n>p+q,正反应为放热反应 |
B. |
m+n>p+q,正反应为吸热反应 |
C. |
m+n<p+q,逆反应为放热反应 |
D. |
m+n<p+q,逆反应为吸热反应 |
|
对于mA(g)+nB(g) | |
A. |
m+n>p+q,正反应是放热反应 |
B. |
m+n>p+q,正反应是吸热反应 |
C. |
m+n<p+q,逆反应是放热反应 |
D. |
m+n<p+q,逆反应是吸热反应 |
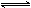 pC(g)+qD(g)的平衡体系,当升高温度时,体系的平均密度对H2的相对密度从16.5变为16.9,则下列说法正确的是
pC(g)+qD(g)的平衡体系,当升高温度时,体系的平均密度对H2的相对密度从16.5变为16.9,则下列说法正确的是