题目内容
14.下列有关说法正确的是( )| A. | 当H2O与Na2O2反应生成1molO2时,转移的电子数目为2×6.02×1023 | |
| B. | 用pH均为2的盐酸和醋酸分别中和等物质的量的NaOH,消耗醋酸的体积更大 | |
| C. | 常温下2S2O(g)═3S(s)+SO2(g)能自发进行,可推断该反应为吸热反应 | |
| D. | 氯水通入SO2后溶液的酸性减弱 |
分析 A.反应2Na2O2+2H2O═4NaOH+O2↑中,只有O元素化合价发生变化,Na2O2既是氧化剂又是还原剂;
B.醋酸为弱酸,等pH时,醋酸浓度大;
C.根据△H-T•△S<0能发生进行判断;
D.二氧化硫具有还原性和氯气发生氧化还原反应生成硫酸和盐酸;
解答 解:A.Na2O2中O元素化合价为-1价,反应中O元素化合价由-1价分别变化为0价和-2价,则Na2O2既是氧化剂又是还原剂,生成1molO2时转移电子2mol即2×6.02×1023,故A正确;
B.醋酸为弱酸,等pH时,醋酸浓度大,分别中和等物质的量的NaOH,消耗醋酸的体积更小,故B错误;
C.反应2S2O(g)═3S(s)+SO2(g),△S<0,如能自发进行,则该反应△H<0时才能满足△H-T•△S<0,所以推断该反应为放热反应,故C错误;
D.SO2通入氯水后,发生反应,Cl2+SO2+2H2O=2HCl+H2SO4,溶液酸性增强,故D错误.
故选A.
点评 本题考查较为综合,涉及氧化还原反应、弱电解质、反应热以及SO2的性质等问题,为高考常见题型,侧重于学生的分析能力的考查,难度不大,注意相关基础知识的积累.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
5.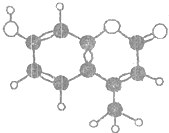 某种激光染料,应用于可调谐染料激光器,它由C、H、O三种元素组成,分子球棍型如图所示,下列有关叙述正确的是①能与溴水发生取代反应 ②能使酸性KMnO4溶液褪色 ③1mol该物质最多能与4mol H2加成 ④1mol该物质最多能与含2mol NaOH的溶液反应( )
某种激光染料,应用于可调谐染料激光器,它由C、H、O三种元素组成,分子球棍型如图所示,下列有关叙述正确的是①能与溴水发生取代反应 ②能使酸性KMnO4溶液褪色 ③1mol该物质最多能与4mol H2加成 ④1mol该物质最多能与含2mol NaOH的溶液反应( )
 某种激光染料,应用于可调谐染料激光器,它由C、H、O三种元素组成,分子球棍型如图所示,下列有关叙述正确的是①能与溴水发生取代反应 ②能使酸性KMnO4溶液褪色 ③1mol该物质最多能与4mol H2加成 ④1mol该物质最多能与含2mol NaOH的溶液反应( )
某种激光染料,应用于可调谐染料激光器,它由C、H、O三种元素组成,分子球棍型如图所示,下列有关叙述正确的是①能与溴水发生取代反应 ②能使酸性KMnO4溶液褪色 ③1mol该物质最多能与4mol H2加成 ④1mol该物质最多能与含2mol NaOH的溶液反应( )| A. | ①②③ | B. | ①③④ | C. | ③④ | D. | ②③④ |
2.重铬酸钾溶液中存在如下平衡:Cr2O72-(橙色)+H2O?2H++2CrO42-(黄色)
①向2mL0.1mol•L-1 K2Cr2O7溶液中滴入3滴6mol•L-1NaOH溶液,溶液由橙色变为黄色;向所得溶液中再滴入5滴浓H2SO4,溶液由黄色变为橙色.
②向2mL 0.1mol•L-1酸化的K2Cr2O7溶液中滴入适量(NH4)2Fe(SO4)2溶液,溶液由橙色变为绿色,发生反应:Cr2O72-+14H++6Fe2+=2Cr3+(绿色)+6Fe3++7H2O.
下列分析正确的是( )
①向2mL0.1mol•L-1 K2Cr2O7溶液中滴入3滴6mol•L-1NaOH溶液,溶液由橙色变为黄色;向所得溶液中再滴入5滴浓H2SO4,溶液由黄色变为橙色.
②向2mL 0.1mol•L-1酸化的K2Cr2O7溶液中滴入适量(NH4)2Fe(SO4)2溶液,溶液由橙色变为绿色,发生反应:Cr2O72-+14H++6Fe2+=2Cr3+(绿色)+6Fe3++7H2O.
下列分析正确的是( )
| A. | 实验①能证明K2Cr2O7溶液中存在上述平衡 | |
| B. | 实验②能说明氧化性:Cr2O72->Fe3+ | |
| C. | CrO42-和Fe2+在酸性溶液中可以大量共存 | |
| D. | 稀释K2Cr2O7溶液时,溶液中各离子浓度均减小 |
9.分析下列实例,根据已有的知识和经验,填写下表.
| 实 例 | 影响速率的因素 | 如何影响 |
| 鲜牛奶变酸:28℃约4h,5℃约48h | ||
| 硫在氧气中比在空气中燃烧快 | ||
| 碳酸钙与盐酸反应:粉状比块状快 | ||
| KClO3与MnO2混合共热可快速产生O2 | ||
| 工业合成氨通常要在高压下进行 | . |
19.下列说法中,正确的是( )
| A. | SO2的摩尔质量是64g | |
| B. | 18g H2O在标准状况下的体积是22.4L | |
| C. | 在标准状况下,20mL NH3 与60mL O2所含的分子数比为1:3 | |
| D. | 将40g NaOH溶于1L水中,所得溶液的物质的量浓度为1mol/L |
6.橙花醛是一种香料,结构简式为(CH3)2C=CHCH2CH2C(CH3)=CHCHO.下列说法正确的是( )
| A. | 橙花醛能够发生氧化反应,不能发生还原反应 | |
| B. | 橙花醛可以使溴水褪色 | |
| C. | 橙花醛是丙烯醛(CH2=CHCHO)是同系物 | |
| D. | 1mol橙花醛最多能与2molH2发生加成反应 |
3.已知反应:①101kPa时,2C(s)+O2(g)═2CO(g)△H=-221kJ/mol; ②稀溶液中,H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ/mol.下列结论正确的是( )
| A. | 碳的燃烧热为221 kJ/mol | |
| B. | 稀硫酸与稀NaOH溶液反应测得中和热为57.3 kJ/mol | |
| C. | 稀硫酸与稀Ba(OH)2溶液反应测得中和热为57.3 kJ/mol | |
| D. | 稀醋酸与稀NaOH溶液反应生成1 mol水时,放出57.3 kJ热量 |
4.某学生以铁丝和Cl2为原料进行下列三个实验.从分类角度分析,下列选项正确的是( )
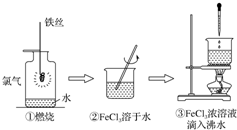

| A. | 实验①、②所涉及的物质均为电解质 | |
| B. | 实验②、③均为放热反应实验 | |
| C. | ②、③均未发生氧化还原反应 | |
| D. | 实验①、③反应制得的物质均为纯净物 |
